题目内容
1.有关反应原理说法错误的是( )| A. | 碳酸钙与盐酸反应过程中,再增加CaCO3固体的量,反应速率不变,但把CaCO3固体粉碎,可以加快反应速率 | |
| B. | 增大反应体系的压强,反应速率不一定增大 | |
| C. | 由温度或压强改变引起的平衡正向移动,反应物的转化率一定增大 | |
| D. | 对于2SO2(g)+O2(g)?2SO3(g)反应,当密度保持不变,在恒温恒容或恒温恒压条件下,均不能作为达到化学平衡状态的标志 |
分析 A.纯固体的量不影响反应速率,但接触面积增大,反应速率增大;
B.压强适用于有气体参加的反应;
C.由温度或压强改变引起的平衡正向移动,反应物的转化程度增大;
D.恒温恒容时密度始终不变,不能判定平衡状态,而恒温恒压条件下,气体体积为变量,密度为变量.
解答 解:A.纯固体的量不影响反应速率,但接触面积增大,反应速率增大,则增加CaCO3固体的量,反应速率不变,但把CaCO3固体粉碎,可以加快反应速率,故A正确;
B.压强适用于有气体参加的反应,对中和反应等压强增大,速率不变,则增大反应体系的压强,反应速率不一定增大,故B正确;
C.由温度或压强改变引起的平衡正向移动,反应物的转化程度增大,则反应物的转化率一定增大,故C正确;
D.恒温恒容时密度始终不变,不能判定平衡状态,而恒温恒压条件下,气体体积为变量,密度为变量,则密度可判定平衡状态,故D错误;
故选D.
点评 本题考查化学平衡,为高频考点,把握反应速率、平衡移动的影响因素为解答的关键,侧重分析与应用能力的考查,注意选项D中平衡判定中利用变量判断,题目难度不大.

练习册系列答案
 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案
相关题目
5.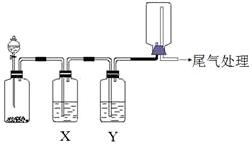 利用图装置可以进行实验并能达到实验目的是( )
利用图装置可以进行实验并能达到实验目的是( )
 利用图装置可以进行实验并能达到实验目的是( )
利用图装置可以进行实验并能达到实验目的是( )| 选项 | 实验目的 | X中试剂 | Y中试剂 |
| A | 用MnO2和浓盐酸制取并收集纯净干燥的Cl2 | 饱和食盐水 | 浓硫酸 |
| B | 用Cu与稀硝酸制取并收集纯净干燥的NO | 水 | 浓硫酸 |
| C | 用CaO于浓氨水制取并收集纯净干燥的NH3 | NaOH溶液 | 碱石灰 |
| D | CaCO3和稀盐酸制取并收集纯净干燥的CO2 | 饱和NaHCO3溶液 | 浓硫酸 |
| A. | A | B. | B | C. | C | D. | D |
6.化学中常用图象直观地描述化学反应的进程或结果.下列图象描述正确的是( )
| A. |  图表示不同压强对反应体系3X(g)?2Y(g)+Z(s)中X体积分数的影响 | |
| B. |  图表示CH3COOH溶液中通入NH3至过量的过程中溶液导电性的变化 | |
| C. |  图中的线条2表示放热反应2H2O2═2H2O+O2加入催化剂Br2的反应进程 | |
| D. |  图表示用0.1000mol•L-1NaOH溶液分别滴定同浓度同体积盐酸和醋酸的曲线 |
9.烷烃C5H12,与氯气发生取代反应所得的一氯取代物没有同分异构体,其结构式为( )
| A. | 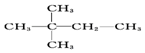 | B. |  | C. | 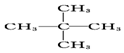 | D. | CH3CH2CH2CH2CH3 |
16.下列叙述中,正确的是( )
| A. | 1 mol H2的质量只有在标准状况下才约为2 g | |
| B. | 在标准状况下,22.4 L由N2、N2O组成的混合气体中所含有的氮原子的物质的量约为2 mol | |
| C. | 在20℃时,1 mol任何气体的体积总比22.4 L大 | |
| D. | 1 mol H2和O2的混合气体,在标准状况下的体积大于22.4 L |
13.锂和镁在元素周期表中有特殊的“对角关系”,它们的单质及其化合物性质相似,下列关于锂及其化合物的叙述中可能正确的是( )
| A. | Li2SO4难溶于水 | B. | LiOH加热时,不会分解 | ||
| C. | Li遇浓H2SO4发生钝化 | D. | Li2CO3加热时,分解成Li2O和CO2 |
10.下列除杂所选用的试剂或操作方法正确的一组是(括号内为杂质)( )
| 选项 | 待提纯的物质 | 除杂的试剂 | 操作方法 |
| A | CO2(HCl) | 饱和NaHCO3溶液 | 洗气 |
| B | Mg(Al) | HCl | 过滤 |
| C | NaCl(NaHCO3) | HCl | 蒸馏 |
| D | 碘水(I2) | 酒精 | 萃取 |
| A. | A | B. | B | C. | C | D. | D |
11.下列说法正确的是( )
| A. | 1 mol蔗糖可以水解生成2mo1葡萄糖 | |
| B. | 食用花生油能发生水解反应 | |
| C. | C2H4C12、C5H12均只有两种同分异构体 | |
| D. | 苯乙烯分子内共平面的碳原子数最多为7个 |