题目内容
5.几种含硅的物质之间相互转化关系如图所示: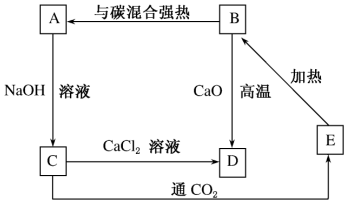
(1)试判断并写出下列物质的化学式:
BSiO2,CNa2SiO3,DCaSiO3,EH2SiO3.
(2)写出下列反应化学方程式
①B→A:SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑;
②B→D:SiO2+CaCO3$\frac{\underline{\;高温\;}}{\;}$CaSiO3+CO2↑;
③C→E:Na2SiO3+CO2+H2O═H2SiO3↓+Na2CO3.
分析 A、B、C、D、E都含硅的物质,A能和碱反应可能为二氧化硅或硅单质,B能和碳单质反应生成A,所以A为Si,B为SiO2,B能和氧化钙反应生成D为CaSiO3,A和氢氧化钠反应生成C为Na2SiO3,Na2SiO3与氯化钙反应生成硅酸钙,Na2SiO3中通入二氧人碳得E为H2SiO3,H2SiO3受热分解得二氧化硅,符合各物质转化关系,以此解答该题.
解答 解:(1)根据上面的分析可知,B为SiO2,C为Na2SiO3,D为CaSiO3,E为H2SiO3,
故答案为:SiO2;Na2SiO3;CaSiO3;H2SiO3;
(2)①B→A的反应为碳还原二氧化硅得硅,反应的方程式为SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑,
故答案为:SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑;
②B→D的反应为二氧化硅与氧化钙在高温条件下得硅酸钙,反应的方程式为SiO2+CaCO3$\frac{\underline{\;高温\;}}{\;}$CaSiO3+CO2↑,
故答案为:SiO2+CaCO3$\frac{\underline{\;高温\;}}{\;}$CaSiO3+CO2↑;
③硅酸钠溶液通入二氧化碳可生产硅酸,反应的化学方程式为Na2SiO3+CO2+H2O═H2SiO3↓+Na2CO3,故答案为:Na2SiO3+CO2+H2O═H2SiO3↓+Na2CO3.
点评 本题考查无机物的推断,为高频考点,注意掌握硅及其化合物之间转化是关键,题目侧重对学生的分析能力的考查,难度中等.

练习册系列答案
 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案
相关题目
9.用下列实验装置进行相应实验,能达到实验目的是( )
| A. | 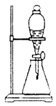 用图所示装置可以将乙醇和水分离 | |
| B. | 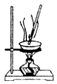 用图所示装置蒸发硫酸铜溶液制备硫酸铜晶体 | |
| C. | 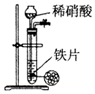 用图所示装置通过稀硝酸与铁反应制取少量的氢气 | |
| D. | 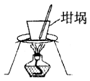 用图所示装置分离氢氧化钙固体中混有的少量氯化铵固体 |
16.下列叙述中,正确的是( )
| A. | 1 mol H2的质量只有在标准状况下才约为2 g | |
| B. | 在标准状况下,22.4 L由N2、N2O组成的混合气体中所含有的氮原子的物质的量约为2 mol | |
| C. | 在20℃时,1 mol任何气体的体积总比22.4 L大 | |
| D. | 1 mol H2和O2的混合气体,在标准状况下的体积大于22.4 L |
13.锂和镁在元素周期表中有特殊的“对角关系”,它们的单质及其化合物性质相似,下列关于锂及其化合物的叙述中可能正确的是( )
| A. | Li2SO4难溶于水 | B. | LiOH加热时,不会分解 | ||
| C. | Li遇浓H2SO4发生钝化 | D. | Li2CO3加热时,分解成Li2O和CO2 |
20.下列有关反应热的叙述中正确的是( )
①已知2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ•mol-1,则氢气的燃烧热为△H=-241.8kJ•mol-1
②由单质A转化为单质B是一个吸热过程,由此可知单质B比单质A稳定
③X(g)+Y(g)?Z(g)+W(s)△H>0,恒温恒容条件下达到平衡后加入X,上述反应的△H增大
④已知:
根据上表数据可以计算出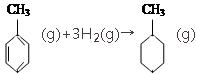 的焓变
的焓变
⑤根据盖斯定律,推知在相同条件下,金刚石或石墨燃烧生成1mol CO2气体时,放出的热量相等
⑥25℃101kPa时,1mol碳完全燃烧生成CO2气体所放出的热量为碳的燃烧热.
①已知2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ•mol-1,则氢气的燃烧热为△H=-241.8kJ•mol-1
②由单质A转化为单质B是一个吸热过程,由此可知单质B比单质A稳定
③X(g)+Y(g)?Z(g)+W(s)△H>0,恒温恒容条件下达到平衡后加入X,上述反应的△H增大
④已知:
| 共价键 | C-C | C═C | C-H | H-H |
| 键能/(kJ•mol-1) | 348 | 610 | 413 | 436 |
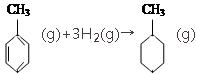 的焓变
的焓变⑤根据盖斯定律,推知在相同条件下,金刚石或石墨燃烧生成1mol CO2气体时,放出的热量相等
⑥25℃101kPa时,1mol碳完全燃烧生成CO2气体所放出的热量为碳的燃烧热.
| A. | ①②③④ | B. | ③④⑤ | C. | ④⑤ | D. | ⑥ |
10.下列除杂所选用的试剂或操作方法正确的一组是(括号内为杂质)( )
| 选项 | 待提纯的物质 | 除杂的试剂 | 操作方法 |
| A | CO2(HCl) | 饱和NaHCO3溶液 | 洗气 |
| B | Mg(Al) | HCl | 过滤 |
| C | NaCl(NaHCO3) | HCl | 蒸馏 |
| D | 碘水(I2) | 酒精 | 萃取 |
| A. | A | B. | B | C. | C | D. | D |
14.下列有关物质用途的说法不正确的是( )
| A. | 聚氯乙烯可用于制食品袋 | B. | 液NH3可用作制冷剂 | ||
| C. | SiO2可用于制造光导纤维 | D. | 漂白粉可用于杀菌消毒 |
15.下列离子方程式正确的是( )
| A. | BaSO3与稀HNO3反应:3BaSO3+2H++2NO3-═3BaSO4+2NO↑+H2O | |
| B. | 碳酸钠溶液中滴加少量氯水的离子方程式为:CO32-+Cl2+H2O=HCO3-+Cl-+HClO | |
| C. | Fe2(SO4)3溶液与Ba(OH)2溶液反应:Fe3++SO42-+Ba2++3OH-═Fe(OH)3↓+BaSO4↓ | |
| D. | 向FeI2溶液中滴加少量氯水,反应的离子方程式为:2Fe2++Cl2═2Fe3++2Cl- |
