题目内容
反应3Fe(S)+4H2O(g)
Fe3O4(s)+4H2(g),在一可变的容积的密闭容器中进行,试回答:
①增加Fe的量,其正反应速率的变化是 (填增大、不变、减小,以下相同)
②将容器的体积缩小一半,其正反应速率 ,逆反应速率 .
③保持体积不变,充入N2使体系压强增大,其正反应速率 ,逆反应速率 .
④保持压强不变,充入N2使容器的体积增大,其正反应速率 ,逆反应速率 .
| ||
①增加Fe的量,其正反应速率的变化是
②将容器的体积缩小一半,其正反应速率
③保持体积不变,充入N2使体系压强增大,其正反应速率
④保持压强不变,充入N2使容器的体积增大,其正反应速率
考点:化学平衡的影响因素
专题:化学平衡专题
分析:根据外界条件对化学反应速率的影响判断,影响化学反应速率的外界因素有温度、浓度、压强、催化剂以及固体的接触面积等等.
解答:
解:①因铁是固体,增加铁的量,没有增加铁的浓度,所以不能改变反应速率,故答案为:不变;
②容器的体积缩小,容器内各物质的浓度都增大,浓度越大,化学反应速率越快,故答案为:增大; 增大;
③体积不变,充入N2使体系压强增大,但各物质的浓度不变,所以反应速率不变,故答案为:不变;不变;
④压强不变,充入N2使容器的体积增大,但各物质的浓度都减小,浓度越小,反应速率越小,故答案为:减小;减小.
②容器的体积缩小,容器内各物质的浓度都增大,浓度越大,化学反应速率越快,故答案为:增大; 增大;
③体积不变,充入N2使体系压强增大,但各物质的浓度不变,所以反应速率不变,故答案为:不变;不变;
④压强不变,充入N2使容器的体积增大,但各物质的浓度都减小,浓度越小,反应速率越小,故答案为:减小;减小.
点评:注意:1、浓度对化学反应速率的影响适用范围是溶液或气体.
2、压强对化学反应速率的影响是通过改变物质的浓度影响的.
3、温度对化学反应速率的影响适用于所有化学反应,无论该反应是放热反应还是吸热反应.
2、压强对化学反应速率的影响是通过改变物质的浓度影响的.
3、温度对化学反应速率的影响适用于所有化学反应,无论该反应是放热反应还是吸热反应.

练习册系列答案
 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案
相关题目
某化学科研小组研究在其他条件不变时,改变某一条件对化学平衡的影响,得到如下变化规律(图中P表示压强,T表示温度,n表示物质的量):根据以上规律判断,下列结论正确的是( )
A、 若反应为2A(g)+B(g)?2C(g),则△H>0,P2>P1 |
B、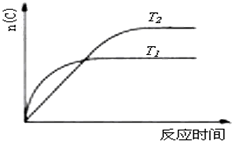 若反应为2A(g)?C(g),则△H>0,T1>T2 |
C、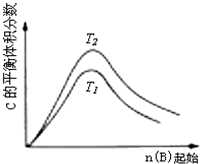 反应为3A(g)+B(g)?2C(g),则△H>0,T2>T1;或△H<0,T2<T1 |
D、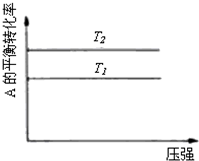 反应为A(g)+B(g)?2C(g),则△H<0,T2>T1 |
某探究小组利用丙酮的溴代反应(CH3COCH3+Br2→CH3COCH2Br+HBr)来研究反应物浓度与反应速率的关系.反应速率v(Br2)通过测定溴的颜色消失所需的时间来确定.在一定温度下,获得如下实验数据:分析实验数据所得出的结论不正确的是( )
| 实验 序号 | 初始浓度c/mol?L-1 | 溴颜色消失 所需时间t/s | ||
| CH3COCH3 | HCl | Br2 | ||
| ① | 0.80 | 0.20 | 0.001 0 | 290 |
| ② | 1.60 | 0.20 | 0.001 0 | 145 |
| ③ | 0.80 | 0.40 | 0.001 0 | 145 |
| ④ | 0.80 | 0.20 | 0.002 0 | 580 |
| A、增大c(CH3COCH3),v(Br2)增大 |
| B、实验②和③的v(Br2)相等 |
| C、增大c(HCl),v(Br2)增大 |
| D、增大c(Br2),v(Br2)增大 |
将如图所示实验装置的K闭合,下列判断正确的是( )
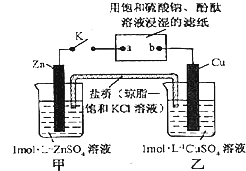

| A、片刻后可观察到滤纸b点变红色 |
| B、电子沿Zn→a→b→Cu路径流动 |
| C、片刻后甲池中c(SO42-)增大 |
| D、Cu电极上发生还原反应 |
将SO2和X气体分别通入BaCl2溶液,未见沉淀生成,若同时通入,有沉淀生成,则X气体不可能是( )
| A、C12 |
| B、NH3 |
| C、CO2 |
| D、NO2 |
在 xR2++y H++O2=4R3++n H2O的离子方程式中,下列判断正确的是( )
| A、y=4,R2+是氧化剂 |
| B、y=2,R2+是还原剂 |
| C、y=2,R3+是还原产物 |
| D、y=4,R3+是氧化产物 |