题目内容
观察A、B、C、D、E五种粒子(原子或离子)的结构示意图,回答有关问题:
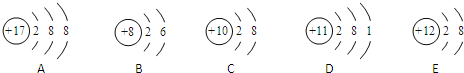
(1)属于离子结构示意图的是 (填字母编号).
(2)性质最稳定的原子是 (填字母编号).
(3)元素D的单质在B2中燃烧,该产物的化学式 .
(4)在核电荷数1-18的元素内,列举两个与C原子的电子层结构相同的离子,写出离子的符号 .
(5)写出化合物DAB在水溶液中的电离方程式 .
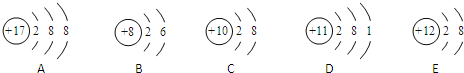
(1)属于离子结构示意图的是
(2)性质最稳定的原子是
(3)元素D的单质在B2中燃烧,该产物的化学式
(4)在核电荷数1-18的元素内,列举两个与C原子的电子层结构相同的离子,写出离子的符号
(5)写出化合物DAB在水溶液中的电离方程式
考点:原子结构示意图
专题:
分析:(1)核电荷数=质子数=核外电子数,为原子;当核电荷数=质子数>核外电子数,为阳离子;当核电荷数=质子数<核外电子数,为阴离子;
(2)元素的化学性质跟它的原子的最外层电子数目关系非常密切,稀有气体性质最稳定;
(3)钠在氧气中燃烧生成过氧化钠;
(4)最外层有10个电子的离子有氧离子、氟离子、钠离子、镁离子、铝离子等;
(5)NaClO是强电解质,强电解质在溶液中能完全电离用“=”,电离出钠离子和次氯酸根离子.
(2)元素的化学性质跟它的原子的最外层电子数目关系非常密切,稀有气体性质最稳定;
(3)钠在氧气中燃烧生成过氧化钠;
(4)最外层有10个电子的离子有氧离子、氟离子、钠离子、镁离子、铝离子等;
(5)NaClO是强电解质,强电解质在溶液中能完全电离用“=”,电离出钠离子和次氯酸根离子.
解答:
解:(1)粒子结构示意图中,圆圈内数字表示核内质子数,弧线表示电子层,弧线上的数字表示该层上的电子数,当核电荷数=质子数>核外电子数,为阳离子,E为镁离子,当核电荷数=质子数<核外电子数,为阴离子,A为氯离子,
故答案为:A、E;
(2)C为惰性气体氖元素,故性质最稳定,故答案为:C;
(3)元素D为钠元素,B为氧元素,钠的单质在O2中燃烧生成过氧化钠,化学式为:Na2O2,故答案为:Na2O2;
(4)最外层有10个电子的离子有氧离子、氟离子、钠离子、镁离子、铝离子等,符号为O2-、F-、Na+、Mg2+、Al3+(任意2个就可),
故答案为:O2-、F-、Na+、Mg2+、Al3+(任意2个就可);
(5)NaClO是强电解质,NaClO在水中电离出钠离子和次氯酸根离子,NaClO═Na++ClO-,故答案为:NaClO=Na++ClO-.
故答案为:A、E;
(2)C为惰性气体氖元素,故性质最稳定,故答案为:C;
(3)元素D为钠元素,B为氧元素,钠的单质在O2中燃烧生成过氧化钠,化学式为:Na2O2,故答案为:Na2O2;
(4)最外层有10个电子的离子有氧离子、氟离子、钠离子、镁离子、铝离子等,符号为O2-、F-、Na+、Mg2+、Al3+(任意2个就可),
故答案为:O2-、F-、Na+、Mg2+、Al3+(任意2个就可);
(5)NaClO是强电解质,NaClO在水中电离出钠离子和次氯酸根离子,NaClO═Na++ClO-,故答案为:NaClO=Na++ClO-.
点评:本题考查学生对粒子结构示意图及其意义的理解、电离方程式的书写等,灵活运用元素周期表中元素的信息、粒子结构示意图的含义是正确解答此类题的关键,题目难度不大.

练习册系列答案
 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案
相关题目
下列仪器①蒸馏烧瓶②试管③蒸发皿④容量瓶⑤冷凝管⑥烧杯中能用酒精灯直接加热的是( )
| A、②③⑤ | B、②③ |
| C、①③④ | D、③⑤⑥ |
某温度下,H2(g)+CO2(g)?H2O(g)+CO(g)的平衡常数K=2.25.该温度下在甲、乙、丙三个恒容密闭容器中,投入H2(g)和CO2(g),其起始浓度如下表所示.下列判断不正确的是( )
| 起始浓度 | 甲 | 乙 | 丙 |
| c(H2)/mol?L-1 | 0.010 | 0.020 | 0.020 |
| c(CO2)/mol?L-1 | 0.010 | 0.010 | 0.020 |
| A、平衡时,乙中CO2、H2的转化率相等 |
| B、平衡时,甲中和丙中H2转化率均是60% |
| C、平衡时,丙中c(CO2)是甲中的2倍,是0.008mol?L-1 |
| D、反应开始时,丙中的反应速率最快,甲中的反应速率最慢 |
食物是维持人类生命和健康的支柱.下表是某食品包装袋上的说明:对上表中各种配料成分的理解不正确的是( )
| 品名 | 蔬菜苏打饼 |
| 配料 | 面粉、鲜鸡蛋、精炼食用植物油、白砂糖、奶油、食盐、脱水青菜、橙汁 |
| 保质期 | 十二个月 |
| 生产日期 | 2008年11月6日 |
| A、富含蛋白质的是鲜鸡蛋 |
| B、富含维生素的是脱水青菜和橙汁 |
| C、富含淀粉的是面粉和白砂糖 |
| D、富含油脂的是精炼食用植物油和奶油 |
下列说法正确的是( )
| A、金属阳离子被还原一定生成金属单质 |
| B、氧化还原反应中有一种元素被氧化,同时一定有另一种元素被还原 |
| C、有单质参加和生成的反应一定是氧化还原反应 |
| D、含有最高化合价的元素的化合物不一定有强氧化性 |
下列物质中,体积为22.4升的是( )
| A、20℃时18g水 |
| B、标准状况下含6.02×1023个原子的Cl2 |
| C、常温常压下1mol氨 |
| D、标准状况下44g二氧化碳 |
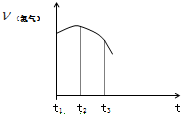 把除去氧化膜的镁条投入到盛有稀盐酸的试管中,产生氢气的速率变化情况如图所示图中t1~t2速率变化的主要原因是
把除去氧化膜的镁条投入到盛有稀盐酸的试管中,产生氢气的速率变化情况如图所示图中t1~t2速率变化的主要原因是