题目内容
2.空气质量报告的各项指标可以反映出各地的空气质量状况.pM2.5即将纳入我国的空气质量报告,pM2.5指的是( )| A. | CO2 | B. | N2 | ||
| C. | NO2 | D. | 直径非常小的可吸入颗粒 |
分析 PM2.5指细颗粒物,细颗粒物指环境空气中空气动力学当量直径小于等于 2.5 微米的颗粒物,属于可吸入颗粒物,据此解答.
解答 解:PM2.5指细颗粒物,属于可吸入颗粒物,细颗粒物指环境空气中空气动力学当量直径小于等于 2.5 微米的颗粒物,
故选:D.
点评 本题考查了环境污染与治理,明确PM2.5的含义是解题关键,题目难度不大.

练习册系列答案
相关题目
12.科学家一直致力于研究常温、常压下“人工固氮”的新方法.曾有实验报道:在常温、常压、光照条件下,N2在催化剂(掺有少量Fe2O3的TiO2)表面与水发生反应,生成的主要产物为NH3.进一步研究NH3生成量与温度的关系,部分实验数据见下表(光照、N2、压强1.0×105 Pa、反应时间3h):
相应的热化学方程式:N2(g)+3H2O(l)?2NH3(g)+$\frac{3}{2}$O2(g)△H=+765.2kJ•mol-1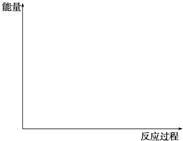
回答下列问题:
(1)请画出上述反应在有催化剂与无催化剂两种情况下反应过程中体系能量变化的示意图,并进行必要标注.
(2)与目前广泛使用的工业合成氨方法相比,该方法固氮反应速率慢.请提出可提高其反应速率且增大NH3生成量的建议:升高温度,增大反应物N2的浓度,不断移出生成物脱离反应体系.
(3)工业合成氨的反应为N2(g)+3H2(g)高温、高压催化剂
2NH3(g).设在容积为2.0L的密闭容器中充入0.60mol N2(g)和1.60mol H2(g),反应在一定条件下达到平衡时,NH3的物质的量分数为$\frac{4}{7}$.
①该条件下N2的平衡转化率为66.7%
②该条件下反应2NH3(g)高温、高压催化剂N2(g)+3H2(g)的平衡常数为0.005.
| T/℃ | 30 | 40 | 50 | 60 |
| NH3生成量/10-6 mol | 4.8 | 5.9 | 6.0 | 6.1 |

回答下列问题:
(1)请画出上述反应在有催化剂与无催化剂两种情况下反应过程中体系能量变化的示意图,并进行必要标注.
(2)与目前广泛使用的工业合成氨方法相比,该方法固氮反应速率慢.请提出可提高其反应速率且增大NH3生成量的建议:升高温度,增大反应物N2的浓度,不断移出生成物脱离反应体系.
(3)工业合成氨的反应为N2(g)+3H2(g)高温、高压催化剂
2NH3(g).设在容积为2.0L的密闭容器中充入0.60mol N2(g)和1.60mol H2(g),反应在一定条件下达到平衡时,NH3的物质的量分数为$\frac{4}{7}$.
①该条件下N2的平衡转化率为66.7%
②该条件下反应2NH3(g)高温、高压催化剂N2(g)+3H2(g)的平衡常数为0.005.
10.下列叙述不正确的是( )
| A. | CH4与C4H10互为同系物 | |
| B. | C5H12有三种同分异构体 | |
| C. | 乙烯、乙醇和乙酸都可以使高锰酸钾溶液褪色 | |
| D. | 苯分子中的碳碳键是介于单键和双键之间的独特的键 |
17.若有2.8g铁完全被锈蚀掉,则O2得到的电子数(NA为阿伏加德罗常数)是( )
| A. | 0.05NA | B. | 0.1NA | ||
| C. | 0.15NA | D. | 条件不足,不能计算 |
7.用NA表示阿伏加德罗常数的值.下列判断正确的是( )
| A. | 常温常压下,18 g 2H2O含有的原子总数目为3NA | |
| B. | 常温常压下,22.4 L Cl2中含有的分子数为NA | |
| C. | 1 mol Na在O2中完全燃烧转移的电子数目为NA | |
| D. | 1 mol•L-1KHSO4溶液中含有的钾离子数目为NA |
14.如图装置能达到对应实验目的是( )
| A. |  收集氢气 | B. |  分离碘和泥沙 | ||
| C. |  分离水和四氯化碳 | D. |  实验室制取蒸馏水 |
12.常温下,下列说法正确的是( )
| A. | 0.1 mol/L的NaHA溶液pH=5,则溶液:c(HA-)>c(H+)>c(A2-)>c(H2A) | |
| B. | 等体积、等物质的量浓度的NaCl(aq) 微粒种类大于NaClO(aq)中微粒种类 | |
| C. | pH=3的硫酸溶液中水的电离程度大于pH=11的氨水溶液中水的电离程度 | |
| D. | 体积相同的0.1 mol/L氨水和0.1 mol/L NaOH溶液中和盐酸的能力后者大 |
