题目内容
11.二氧化钛广泛应用于各类结构表面涂料、纸张涂层等,二氧化钛还可作为制备钛单质的原料.二氧化钛可由以下两种方法制备:方法1:TiCl4水解生成TiO2•xH2O,过滤、水洗除去其中的Cl-,再烘干、焙烧除去水分得到粉体TiO2,此方法制备得到的是纳米二氧化钛.
①TiCl4水解生成TiO2•x H2O的化学方程式为TiCl4+(x+2)H2O$\frac{\underline{\;\;△\;\;}}{\;}$ TiO2•xH2O↓+4HCl;
②检验TiO2•x H2O中Cl-是否被除净的方法是取最后一次洗涤液,滴加硝酸酸化的AgNO3溶液,不产生白色沉淀,说明Cl-已除净.
方法2:可用含有Fe2O3的钛铁矿(主要成分为FeTiO3,其中Ti元素化合价为+4价)制取,其主要流程如图:

(1)甲溶液中除含TiO2+之外还含有的金属阳离子有Fe3+、Fe2+.
(2)加Fe的作用是将Fe3+转化为Fe2+.
(3)TiO2制取单质Ti,涉及到的步骤如下:
TiO2$\stackrel{①}{→}$TiCl4$→_{②}^{800℃}$Ti
反应②的方程式是TiCl4+2Mg$\frac{\underline{\;800℃\;}}{\;}$2MgCl2+Ti,该反应需要在Ar气氛中进行,请解释原因:防止高温下Mg(Ti)与空气中的O2(或CO2、N2)作用.
分析 方法1.①加热条件下,四氯化钛水解生成TiO2•xH2O和HCl,升高温度促进四氯化钛水解和盐酸挥发;
②氯离子用硝酸酸化的硝酸银溶液检验;
方法2.钛铁矿和过量稀硫酸混合,FeTiO3和稀硫酸反应生成Fe2+、TiO2+,氧化铁和稀硫酸反应生成Fe3+,所以溶液甲中含有Fe2+、TiO2+、Fe3+,然后向溶液中加入Fe,Fe将Fe3+氧化生成Fe2+,然后过滤得到滤渣和滤液,将滤液蒸发浓缩、冷却结晶得到绿矾和含有TiO2+溶液乙,通过一系列反应得到TiO2;
(1)氧化铁和稀硫酸反应生成铁离子、铁离子和Fe反应生成亚铁离子;
(2)铁离子具有氧化性,能氧化铁生成亚铁离子;
(3)在800℃条件下,四氯化钛和镁反应生成氯化镁和钛,Mg是活泼金属,能与空气中多种物质反应,因此可得出Ar气作用为保护气,防止Mg和空气中物质反应.
解答 解:方法1.①加热条件下,四氯化钛水解生成TiO2•xH2O和HCl,升高温度促进四氯化钛水解和盐酸挥发,所以蒸干溶液时得到TiO2•x H2O,化学反应方程式为TiCl4+(x+2)H2O$\frac{\underline{\;\;△\;\;}}{\;}$ TiO2•xH2O↓+4HCl,故答案为:TiCl4+(x+2)H2O$\frac{\underline{\;\;△\;\;}}{\;}$ TiO2•xH2O↓+4HCl;
②氯离子用硝酸酸化的硝酸银溶液检验,其检验方法为取最后一次洗涤液,滴加硝酸酸化的AgNO3溶液,不产生白色沉淀,说明Cl-已除净,
故答案为:取最后一次洗涤液,滴加硝酸酸化的AgNO3溶液,不产生白色沉淀,说明Cl-已除净;
方法2.钛铁矿和过量稀硫酸混合,FeTiO3和稀硫酸反应生成Fe2+、TiO2+,氧化铁和稀硫酸反应生成Fe3+,所以溶液甲中含有Fe2+、TiO2+、Fe3+,然后向溶液中加入Fe,Fe将Fe3+氧化生成Fe2+,然后过滤得到滤渣和滤液,将滤液蒸发浓缩、冷却结晶得到绿矾和含有TiO2+溶液乙,通过一系列反应得到TiO2;
(1)氧化铁和稀硫酸反应生成铁离子、铁离子和Fe反应生成亚铁离子,所以甲溶液中还含有Fe3+、Fe2+,故答案为:Fe3+、Fe2+;
(2)铁离子具有氧化性,能氧化铁生成亚铁离子,同时将Fe3+转化为Fe2+,故答案为:将Fe3+转化为Fe2+;
(3)在800℃条件下,四氯化钛和镁反应生成氯化镁和钛,反应方程式为TiCl4+2Mg$\frac{\underline{\;800℃\;}}{\;}$2MgCl2+Ti;Mg是活泼金属,能与空气中多种物质反应,因此可得出Ar气作用为保护气,防止Mg和空气中物质反应,故答案为:TiCl4+2Mg$\frac{\underline{\;800℃\;}}{\;}$2MgCl2+Ti;防止高温下Mg(Ti)与空气中的O2(或CO2、N2)作用.
点评 本题考查物质制备,为高频考点,明确物质性质、物质分离和提纯方法是解本题关键,同时考查学生获取信息、运用信息解答问题能力,知道流程图中每一步发生的反应,题目难度不大.

| A. | 使用有少量蒸馏水的容量瓶配制溶液 | |
| B. | NaOH溶解后未冷却到室温即转移至容量瓶 | |
| C. | 移液后烧杯未用蒸馏水洗涤 | |
| D. | 定容时俯视液面 |
| A. | CO2 | B. | N2 | ||
| C. | NO2 | D. | 直径非常小的可吸入颗粒 |
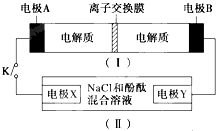 如图装置(Ⅰ)为一种可充电电池的示意图,其中的离子交换膜只允许K+通过,该电池充放电的化学方程式为;2K2S2+KI3$?_{充电}^{放电}$K2S4+3KI,装置(Ⅱ)为电解池的示意图当闭合开关K时,X附近溶液先变红.则下列说法正确的是( )
如图装置(Ⅰ)为一种可充电电池的示意图,其中的离子交换膜只允许K+通过,该电池充放电的化学方程式为;2K2S2+KI3$?_{充电}^{放电}$K2S4+3KI,装置(Ⅱ)为电解池的示意图当闭合开关K时,X附近溶液先变红.则下列说法正确的是( )| A. | 闭合K时,K十从左到右通过离子交换膜 | |
| B. | 闭合K时,A的电极反应式为:3I--2e-═I2- | |
| C. | 闭合K时,X的电极反应式为:2CI--2e-═Cl2↑个 | |
| D. | 闭合K时,当有0.1mo1K+通过离子交换膜,X电极上产生标准状况下气体2.24L |
| A. | 硫酸的摩尔质量是98 g | B. | 18 g水中含有水分子数为NA | ||
| C. | O2的摩尔质量等于其相对分子质量 | D. | 1 mol CO的质量为28 g•mol-1 |
 某小组同学用如图装置进行实验研究(a、b、c表示止水夹).请评价或完善其方案:
某小组同学用如图装置进行实验研究(a、b、c表示止水夹).请评价或完善其方案:(1)将装置A、C、E相连接,用MnO2和浓盐酸制取氯气,请回答:
①A中反应的离子方程式:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++2H2O+Cl2↑;.
②E中氢氧化钠溶液的作用吸收多余的Cl2.
在C中加入适量的水可制得氯水.将所得氯水分成两份进行实验,其操作、现象和结论如表:
| 实验序号 | 实验操作 | 现象 | 结论 |
| Ⅰ | 将氯水滴入品红溶液 | 品红溶液褪色 | 氯气有漂白性 |
| Ⅱ | 氯水中加入碳酸氢钠粉末 | 有无色气泡产生 | 氯气与水反应的产物具有酸性 |
④.实验Ⅱ推出相应的结论是否合理?不合理,若不合理,请说明理由(若合理,无需填写)制取的氯气中含HCl气体,其溶于水能与NaHCO3粉末反应产生气泡.
(2)将B、D、E相连,在B中装浓硝酸和铜片,可制得NO2并进行有关实验.
①B中反应的化学方程式Cu+4HNO3(浓)═Cu(NO3)2+2NO2↑+2H2O.
②先若关闭c,当丁中充满红棕色的NO2时,再关闭止水夹a、b,微热试管丁,丁中可观察到的实验现象丁中气体的红棕色变深.
| A. | HCl水溶液是强酸,任何强酸都导致有沉淀析出 | |
| B. | Cl-浓度增大,使平衡向生成氯化钠的方向移动,生成NaCl(s) | |
| C. | 酸的存在降低了Ksp(NaCl)的数值 | |
| D. | Ksp(NaCl)不受酸的影响,但增加Cl-浓度,能使Ksp(NaCl)减小 |
| A. | 实验结束后将所有的废液倒入下水道排出实验室,以免污染实验室 | |
| B. | 为了使养分还田而将植物秸秆焚烧处理 | |
| C. | PM2.5是指大气中直径接近于2.5×10-6m(1m=109nm)的颗粒物,这些细颗粒物分散在空气中形成的分散系是胶体 | |
| D. | 实现资源的“3R”利用,即:减少资源消耗(Reduce)、增加资源的重复使用(Reuse)、提高资源的循环利用(Recycle) |