题目内容
下列框图中A、F、G、H都是芳香族化合物.A的相对分子质量不超过200,完全燃烧只生成CO2和H2O;A中氧元素的质量分数为
.
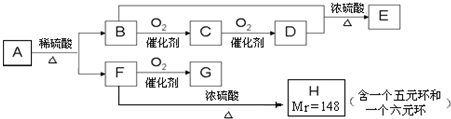
又已知:①E能发生银镜反应,G不能发生银镜反应;②F与FeCl3溶液不显紫色.回答下列问题:
(1)下列叙述正确的是 .
(A)A的分子式是C10H14O3 (B)A能发生氧化、还原、取代、消去等反应
(C)1mol A最多能与3mol H2发生加成反应 (D)A能与NaHCO3溶液反应放出CO2
(2)F分子中含有的官能团的名称是: .
(3)由F转化成H的反应类型属于 .
(4)写出B+D→E的化学方程式: .
(5)写出F→G的化学方程式: .
(6)H的同分异构体甚多.请写出符合下列条件的同分异构体的结构简式(任写三种): .
①苯环上只有一个链状取代基; ②能够与NaOH溶液反应.
| 8 |
| 30 |

又已知:①E能发生银镜反应,G不能发生银镜反应;②F与FeCl3溶液不显紫色.回答下列问题:
(1)下列叙述正确的是
(A)A的分子式是C10H14O3 (B)A能发生氧化、还原、取代、消去等反应
(C)1mol A最多能与3mol H2发生加成反应 (D)A能与NaHCO3溶液反应放出CO2
(2)F分子中含有的官能团的名称是:
(3)由F转化成H的反应类型属于
(4)写出B+D→E的化学方程式:
(5)写出F→G的化学方程式:
(6)H的同分异构体甚多.请写出符合下列条件的同分异构体的结构简式(任写三种):
①苯环上只有一个链状取代基; ②能够与NaOH溶液反应.
考点:有机物的推断
专题:有机物的化学性质及推断
分析:B经过两步氧化生成D,且D和B反应生成E,E能发生银镜反应,则D为HCOOH,B为CH3OH,E为HCOOCH3,C为HCHO,F能被氧化成G,F与FeCl3溶液不显紫色,即没有酚羟基,说明F中有醇羟基,G不能发生银镜反应,说明F中不含-CH2OH,F在浓硫酸的作用下,生成H,说明F中有羧基,则A中应有酯基和羟基,至少含3个氧原子,此时A的相对分子质量为
=180,不超过200,所以A中一定含有3个氧原子.因为A中含有苯环和酯基,因此判断A的不饱和度为5,因此可以设A的分子式为CnH2n-8O3,结合相对分子质量为180判断A的分子式为C10H12O3,A分子中含有苯环、酯基、羟基,又H含有一个六元环和一个五元环,因此判断H为F发生分子内脱水的产物,综合分析知A的结构简式为 ,所以F为
,所以F为 ,G为
,G为 ,以此解答该题.
,以此解答该题.
| 3×16 | ||
|
 ,所以F为
,所以F为 ,G为
,G为 ,以此解答该题.
,以此解答该题.解答:
解:B经过两步氧化生成D,且D和B反应生成E,E能发生银镜反应,则B为CH3OH,E为HCOOCH3,C为HCHO,F能被氧化成G,F与FeCl3溶液不显紫色,即没有酚羟基,说明F中有醇羟基,G不能发生银镜反应,说明F中不含-CH2OH,F在浓硫酸的作用下,生成H,说明F中有羧基,则A中应有酯基和羟基,至少含3个氧原子,此时A的相对分子质量为
=180,不超过200,所以A中一定含有3个氧原子.因为A中含有苯环和酯基,因此判断A的不饱和度为5,因此可以设A的分子式为CnH2n-8O3,结合相对分子质量为180判断A的分子式为C10H12O3,A分子中含有苯环、酯基、羟基,又H含有一个六元环和一个五元环,因此判断H为F发生分子内脱水的产物,综合分析知A的结构简式为 ,所以F为
,所以F为 ,G为
,G为 ,
,
(1)(A)由上面的分析可知,A的分子式是C10H12O3,故错误;
(B)A为 ,能发生氧化、还原、取代、消去等反应,故正确;
,能发生氧化、还原、取代、消去等反应,故正确;
(C)1mol A最多能与3mol H2在苯环上发生加成反应,故正确;
(D)A中没有羧基,所以不能与NaHCO3溶液反应放出CO2,故错误;
故选BC;
(2)F为 ,所以F分子中含有的官能团为羟基、羧基,
,所以F分子中含有的官能团为羟基、羧基,
故答案为:羟基、羧基;
(3)由F转化成H是分子内形成酯,是取代(酯化)反应,
故答案为:取代(酯化)反应;
(4)B+D→E的化学方程式为CH3OH+HCOOH
HCOOCH3+H2O,
故答案为:CH3OH+HCOOH
HCOOCH3+H2O;
(5)F→G的化学方程式为 ,
,
故答案为: ;
;
(6)H的同分异构体中符合①苯环上只有一个链状取代基;②能够与NaOH溶液反应,可以有酯基或羧基,其结构简式有 ,
,
故答案为: .
.
| 3×16 | ||
|
 ,所以F为
,所以F为 ,G为
,G为 ,
,(1)(A)由上面的分析可知,A的分子式是C10H12O3,故错误;
(B)A为
 ,能发生氧化、还原、取代、消去等反应,故正确;
,能发生氧化、还原、取代、消去等反应,故正确;(C)1mol A最多能与3mol H2在苯环上发生加成反应,故正确;
(D)A中没有羧基,所以不能与NaHCO3溶液反应放出CO2,故错误;
故选BC;
(2)F为
 ,所以F分子中含有的官能团为羟基、羧基,
,所以F分子中含有的官能团为羟基、羧基,故答案为:羟基、羧基;
(3)由F转化成H是分子内形成酯,是取代(酯化)反应,
故答案为:取代(酯化)反应;
(4)B+D→E的化学方程式为CH3OH+HCOOH
| 浓硫酸 |
| △ |
故答案为:CH3OH+HCOOH
| 浓硫酸 |
| △ |
(5)F→G的化学方程式为
 ,
,故答案为:
 ;
;(6)H的同分异构体中符合①苯环上只有一个链状取代基;②能够与NaOH溶液反应,可以有酯基或羧基,其结构简式有
 ,
,故答案为:
 .
.
点评:本题考查有机物的推断,题目难度中等,对学生的逻辑推理有较高的要求,熟练掌握官能团的结构和性质,根据F发生的反应结合A中元素的质量分数判断A含有个氧原子数目是解题关键.

练习册系列答案
相关题目