题目内容
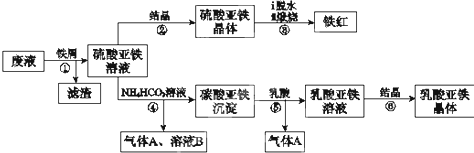
亚硫酸盐是一种常见食品添加剂.为检验某食品中亚硫酸盐含量(通常1kg样品中含SO2的质量计),某研究小组设计了如下两种实验流程:
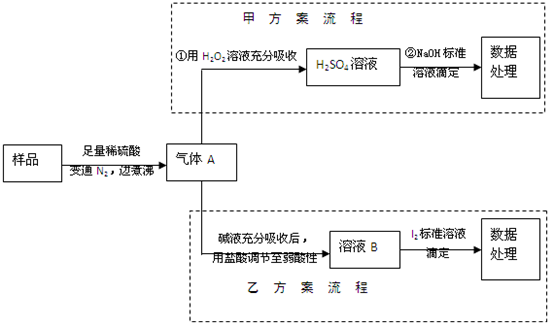
回答下列问题
(1)气体A的主要成分是 ,为防止煮沸时发生暴沸,必须先向烧瓶中加入 ;通入N2的目的是 .
(2)写出甲方案第①步反应的离子方程式: .
(3)甲方案第②步滴定前俯视读数,滴定后仰视读数实验测定的结果 (填“偏高”、“偏低”或“无影响”)
(4)若用盐酸代替稀硫酸处理样品,则按乙方案实验测定的结果 (填“偏高”、“偏低”或“无影响”)
(5)若取样品wg,按乙方案测得消耗0.01000mol?L-1I2溶液VmL,则1kg样品中含SO2的质量是 g(用含w、V的代数式表示).

回答下列问题
(1)气体A的主要成分是
(2)写出甲方案第①步反应的离子方程式:
(3)甲方案第②步滴定前俯视读数,滴定后仰视读数实验测定的结果
(4)若用盐酸代替稀硫酸处理样品,则按乙方案实验测定的结果
(5)若取样品wg,按乙方案测得消耗0.01000mol?L-1I2溶液VmL,则1kg样品中含SO2的质量是
考点:探究物质的组成或测量物质的含量
专题:实验探究和数据处理题
分析:(1)亚硫酸盐与稀硫酸反应生成气体SO2,反应时加入碎瓷片防止暴沸,要保证SO2全部赶出.
(2)SO2具有还原性,可被氧化剂H2O2所氧化;
(3)根据滴定原理进行误差分析;
(4)根据SO2用碱液吸收后需再用盐酸调节溶液至弱酸性分析;
(5)利用关系式法计算.
(2)SO2具有还原性,可被氧化剂H2O2所氧化;
(3)根据滴定原理进行误差分析;
(4)根据SO2用碱液吸收后需再用盐酸调节溶液至弱酸性分析;
(5)利用关系式法计算.
解答:
解:(1)亚硫酸盐与稀硫酸反应生成气体SO2,为防止液体加热时暴沸,一般可加入碎瓷片,因定量实验,需考查减小实验操作误差,通入N2可将生成的SO2全部赶出,保证被吸收液全部吸收,
故答案为:SO2;碎瓷片;将生成的SO2全部赶出,防止SO2在水溶液中被O2氧化;
(2)SO2具有还原性,可被氧化剂H2O2所氧化,反应的离子方程式为SO2+H2O2=SO42-+2H+,
故答案为:SO2+H2O2=SO42-+2H+;
(3)甲方案第②步用NaOH溶液滴定,滴定前俯视读数,滴定后仰视读数实验测定,导致NaOH溶液的体积读数偏大,根据滴定原理,可知实验测定的结果
偏高;
故答案为:偏高;
(4)用盐酸代替硫酸,生成的SO2气体中混有少量HCl,因SO2用碱液吸收后需再用盐酸调节溶液至弱酸性,因此混合气体中含有HCl,对实验结果无影响,
故答案为:无影响;
(5)反应的离子方程式为H2O+SO32-+I2=SO42-+2H++2I-,SO2~SO32-~I2,
64g 1mol
m 0.01000mol?L-1×V×10-3L=10-5mol
m=64×V×10-5g,则1kg样品中含SO2的质量为
=
,
故答案为:
.
故答案为:SO2;碎瓷片;将生成的SO2全部赶出,防止SO2在水溶液中被O2氧化;
(2)SO2具有还原性,可被氧化剂H2O2所氧化,反应的离子方程式为SO2+H2O2=SO42-+2H+,
故答案为:SO2+H2O2=SO42-+2H+;
(3)甲方案第②步用NaOH溶液滴定,滴定前俯视读数,滴定后仰视读数实验测定,导致NaOH溶液的体积读数偏大,根据滴定原理,可知实验测定的结果
偏高;
故答案为:偏高;
(4)用盐酸代替硫酸,生成的SO2气体中混有少量HCl,因SO2用碱液吸收后需再用盐酸调节溶液至弱酸性,因此混合气体中含有HCl,对实验结果无影响,
故答案为:无影响;
(5)反应的离子方程式为H2O+SO32-+I2=SO42-+2H++2I-,SO2~SO32-~I2,
64g 1mol
m 0.01000mol?L-1×V×10-3L=10-5mol
m=64×V×10-5g,则1kg样品中含SO2的质量为
| 64×V×10-5g×1000 |
| w |
| 0.64V |
| w |
故答案为:
| 0.64V |
| w |
点评:本题属工业流程题以食品中的亚硫酸盐含量的测定为问题情境,通过简明的实验流程图,将实验基本操作、仪器的使用、化学计算、化学方程式的书写等内容综合在一起,考查考生对化学实验方案的分析和问题解决的能力,题目难度中等.

练习册系列答案
 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案
相关题目
在配制一定物质的量浓度的NaOH溶液时,下列哪个原因会造成所配溶液浓度偏高( )
| A、所用NaOH已经潮解 |
| B、向容量瓶中加水未到刻度线 |
| C、有少量NaOH溶液残留在烧杯里 |
| D、所用容量瓶不干燥 |
下列表示的是有机化合物结构式中的一部分,其中不是官能团的是( )
| A、-OH |
B、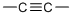 |
C、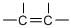 |
| D、-CH3 |
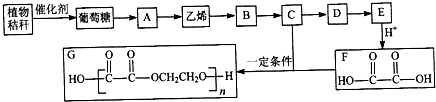
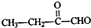 的合成路线流程图(无极试剂任用),合成路线流程图示例如下:CH3CH2OH
的合成路线流程图(无极试剂任用),合成路线流程图示例如下:CH3CH2OH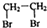

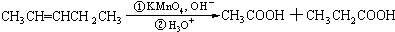
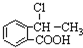 合成
合成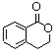 ,写出相关合成流程图(无机试剂任取).
,写出相关合成流程图(无机试剂任取).