��Ŀ����
�±��г��˳������������������ַ���
��1������[CO��NH2��2]��NO��NO2���ߵ����ʵ�����Ӧ�Ļ�ѧ����ʽΪ ��
��2����֪��N2��g��+O2��g���T2NO��g����H=+180.6kJ?mol-1
N2��g��+3H2��g��=2NH3��g����H=-92.4kJ?mol-1
2H2��g��+O2��g���T2H2O��g����H=-483.6kJ?mol-1
��4NO��g��+4NH3��g��+O2��g���T4N2��g��+6H2O��g����H= kJ?mol-1��
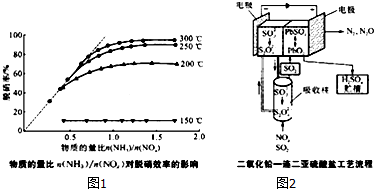
��3�������뵪������������ʵ���֮�ȶ�������Ӱ����ͼ1����ͼ��֪�������˵��¶��� ��
��4��������Ǧһ�����������ι����ǵ¹���ѧ�豸Э�Ὺ���ĵ��͵绯ѧӦ����������I�գ��乤�����̼�ͼ2���ڵ��ģʽʱ�������������յĵ缫��ӦʽΪ ��
��5����������������ʵ���Ũ�ȵĴ�������Һ������������Һ��ϣ���Ӧ����Һ�и�������Ũ���ɴ�С��˳��Ϊ ��
��6�������£���һ�������0.1mol?Lһ1������������Һ�м���һ�����0.1mol/L���������Һ��pH=12����Ӧ����Һ�����������ԭ��������Һ���֮�ͣ�������������Һ�������������� ��
| ��� | ���� | ԭ�� |
| ����һ | ���ط� | ���¶�70-95��ʱ��������Һ����NO��NO2������ת��ΪN2 |
| ������ | ѡ���Դ���ԭ�� SCR���� | ��NH3����Ϊ��ԭ�����������е�NOx��ԭ����N2��H2O |
| ������ | ��ѧ�� | ��������������Ϊ������ԭ�н������NOx��ԭΪN2��N2O�������������α�������SO32-�����绯ѧ��ԭ���ظ�ʹ�ã������ڵ��ģʽ��SO2����Ϊ���ᣬ������ģʽʱ����ؿ����� |
��2����֪��N2��g��+O2��g���T2NO��g����H=+180.6kJ?mol-1
N2��g��+3H2��g��=2NH3��g����H=-92.4kJ?mol-1
2H2��g��+O2��g���T2H2O��g����H=-483.6kJ?mol-1
��4NO��g��+4NH3��g��+O2��g���T4N2��g��+6H2O��g����H=
��3�������뵪������������ʵ���֮�ȶ�������Ӱ����ͼ1����ͼ��֪�������˵��¶���

��4��������Ǧһ�����������ι����ǵ¹���ѧ�豸Э�Ὺ���ĵ��͵绯ѧӦ����������I�գ��乤�����̼�ͼ2���ڵ��ģʽʱ�������������յĵ缫��ӦʽΪ
��5����������������ʵ���Ũ�ȵĴ�������Һ������������Һ��ϣ���Ӧ����Һ�и�������Ũ���ɴ�С��˳��Ϊ
��6�������£���һ�������0.1mol?Lһ1������������Һ�м���һ�����0.1mol/L���������Һ��pH=12����Ӧ����Һ�����������ԭ��������Һ���֮�ͣ�������������Һ��������������
���㣺�ø�˹���ɽ����йط�Ӧ�ȵļ���,��ѧ��Դ���͵��,����Ũ�ȴ�С�ıȽ�,�����ʱ�Ķ����жϼ��й�ph�ļ���
ר�⣺��ѧ��Ӧ�е������仯,����ƽ������Һ��pHר��,�绯ѧר��
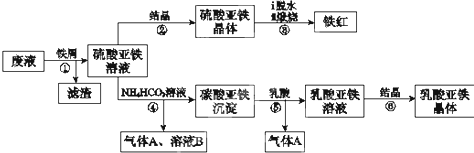
��������1������[CO��NH2��2]��NO��NO2���ߵ����ʵ�����Ӧ���ɵ�����������̼��ˮ������ԭ���غ���д��ѧ����ʽ��
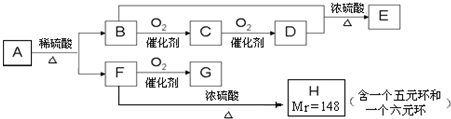
��2�������Ȼ�ѧ����ʽ��˹���ɼ���õ������Ȼ�ѧ����ʽ��
��3��װ��ͼ��֪�¶�Ϊ300��Cʱ�������ʽӽ�100%��
��4��װ��ͼ������������ʧ���ӱ������������
��5����������������ʵ���Ũ�ȵĴ�������Һ������������Һ��ϣ�ǡ�÷�Ӧ���������ƺʹ��ᣬ��ϴ�����������ʷ���Ƭ����Ũ�ȴ�С��
��6������H++OH-=H2O����һ�������0.1mol?Lһ1������������Һ�м���һ�����0.1mol/L���������Һ��pH=12��˵����Һ�Լ��ԣ����ʣ������������Ũ�ȼ���õ���Һ����ȣ�
��2�������Ȼ�ѧ����ʽ��˹���ɼ���õ������Ȼ�ѧ����ʽ��
��3��װ��ͼ��֪�¶�Ϊ300��Cʱ�������ʽӽ�100%��
��4��װ��ͼ������������ʧ���ӱ������������
��5����������������ʵ���Ũ�ȵĴ�������Һ������������Һ��ϣ�ǡ�÷�Ӧ���������ƺʹ��ᣬ��ϴ�����������ʷ���Ƭ����Ũ�ȴ�С��
��6������H++OH-=H2O����һ�������0.1mol?Lһ1������������Һ�м���һ�����0.1mol/L���������Һ��pH=12��˵����Һ�Լ��ԣ����ʣ������������Ũ�ȼ���õ���Һ����ȣ�
���
�⣺��1������[CO��NH2��2]��NO��NO2���ߵ����ʵ�����Ӧ���ɵ�����������̼��ˮ������ԭ���غ���д��ѧ����ʽ����Ӧ�Ļ�ѧ����ʽΪ��NO+NO2+CO��NH2��2=2H2O+CO2+2N2��
�ʴ�Ϊ��NO+NO2+CO��NH2��2=2H2O+CO2+2N2 ��
��2����֪����N2��g��+O2��g���T2NO��g����H=+180.6kJ?mol-1
��N2��g��+3H2��g��=2NH3��g����H=-92.4kJ?mol-1
��2H2��g��+O2��g���T2H2O��g����H=-483.6kJ?mol-1
���ݸ�˹���ɢۡ�3-�ڡ�2-�١�2�õ���4NO��g��+4NH3��g��+O2��g���T4N2��g��+6H2O��g����H=-1627.2KJ/mol��
�ʴ�Ϊ��-1627.2��
��3������ͼ���֪�¶�Ϊ300��Cʱ�������뵪������������ʵ���֮��1��1�������ʽӽ�100%���
�ʴ�Ϊ��300��C��
��4��װ��ͼ�������ù������ڵ�غ����ص�ģʽ��ϣ��ڵ��ģʽ�£���������ʧ���ӱ�������������缫��ӦΪ��SO2+2H2O-2e-=4H++SO42-��
�ʴ�Ϊ��SO2+2H2O-2e-=4H++SO42-��
��5����������������ʵ���Ũ�ȵĴ�������Һ������������Һ��ϣ�ǡ�÷�Ӧ���������ƺʹ��ᣬ��ϴ�����������ʷ�������Һ�����ԣ�c��Na+����c��SO42-����c��H+����c��CH3COO-����c��OH-����
�ʴ�Ϊ��c��Na+����c��SO42-����c��H+����c��CH3COO-����c��OH-����
��6�������£���һ�������0.1mol?Lһ1������������Һ�м���һ�����0.1mol/L���������Һ��pH=12����Һ�Լ��ԣ���Ӧ����Һ�����������ԭ��������Һ���֮�ͣ�
��c��OH-��=
=10-2mol/L
V�����V���ᣩ=11��9
�ʴ�Ϊ��11��9��
�ʴ�Ϊ��NO+NO2+CO��NH2��2=2H2O+CO2+2N2 ��
��2����֪����N2��g��+O2��g���T2NO��g����H=+180.6kJ?mol-1
��N2��g��+3H2��g��=2NH3��g����H=-92.4kJ?mol-1
��2H2��g��+O2��g���T2H2O��g����H=-483.6kJ?mol-1
���ݸ�˹���ɢۡ�3-�ڡ�2-�١�2�õ���4NO��g��+4NH3��g��+O2��g���T4N2��g��+6H2O��g����H=-1627.2KJ/mol��
�ʴ�Ϊ��-1627.2��
��3������ͼ���֪�¶�Ϊ300��Cʱ�������뵪������������ʵ���֮��1��1�������ʽӽ�100%���
�ʴ�Ϊ��300��C��
��4��װ��ͼ�������ù������ڵ�غ����ص�ģʽ��ϣ��ڵ��ģʽ�£���������ʧ���ӱ�������������缫��ӦΪ��SO2+2H2O-2e-=4H++SO42-��
�ʴ�Ϊ��SO2+2H2O-2e-=4H++SO42-��
��5����������������ʵ���Ũ�ȵĴ�������Һ������������Һ��ϣ�ǡ�÷�Ӧ���������ƺʹ��ᣬ��ϴ�����������ʷ�������Һ�����ԣ�c��Na+����c��SO42-����c��H+����c��CH3COO-����c��OH-����
�ʴ�Ϊ��c��Na+����c��SO42-����c��H+����c��CH3COO-����c��OH-����
��6�������£���һ�������0.1mol?Lһ1������������Һ�м���һ�����0.1mol/L���������Һ��pH=12����Һ�Լ��ԣ���Ӧ����Һ�����������ԭ��������Һ���֮�ͣ�
��c��OH-��=
| V(��)��0.1mol/L-0.1mol/L��V(��) |
| V(��)+V(��) |
V�����V���ᣩ=11��9
�ʴ�Ϊ��11��9��
���������⿼�����Ȼ�ѧ����ʽ��˹���ɼ���Ӧ�ã��������Һ��Ϻ�����Ũ�ȴ�С�ȽϷ�������Ӧ����Һ������Ũ�ȵļ�����������ջ����ǹؼ�����Ŀ�Ѷ��еȣ�

��ϰ��ϵ�д�
 ��ĩ�����ϵ�д�
��ĩ�����ϵ�д�
�����Ŀ
��֪��ӡ������ʱ�ײ�������������Ũ�ȹ���ʱ�������к�����������ǿ�����ԣ�����ʹʪ��⻯�ص�����ֽ���������г�������ת�������������ڸ÷�Ӧ��˵����ȷ���ǣ�������
| A���÷�Ӧ�����ӷ���ʽΪ��2I-+O3+H2O�T2OH-+I2+O2 |
| B����Ӧ��ÿ1mol�����μӷ�Ӧ����ת����Ϊ6mol |
| C��O2�Ǹ÷�Ӧ�Ļ�ԭ���� |
| D���ɸ÷�Ӧ��֪�����ԵĴ�С˳��O3��O2 |
�Ҵ����Է������з�Ӧ���ڷ�Ӧ���Ҵ����Ӷ���C-O����ʧȥ�ǻ����ǣ�������
| A���Ҵ���Ũ��������·�����ȥ��Ӧ |
| B���Ҵ�������Ʒ�Ӧ |
| C���Ҵ���������Ӧ |
| D���Ҵ���ͭ˿���������·��������� |
 ��
��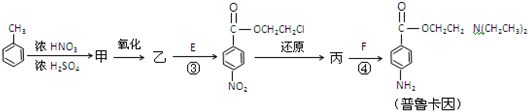

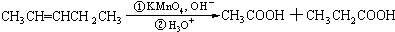
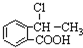 �ϳ�
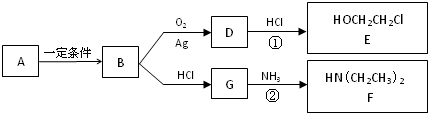
�ϳ�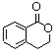 ��д����غϳ�����ͼ�����Լ���ȡ����
��д����غϳ�����ͼ�����Լ���ȡ����