题目内容
17.设NA为阿伏加德罗常数的值,下列说法正确的是( )| A. | 常温常压下,14g由N2与CO组成的混合气体含有的原子数目为NA | |
| B. | 常温常压下,1molNO2气体与水完全反应,转移电子数为NA | |
| C. | 标准状况下,11.2LC2H5OH中所含的分子数为0.5NA | |
| D. | 常温常压下,17gNH3中含有的共用电子对数为4NA |
分析 A.氮气和一氧化碳的摩尔质量都是28g/mol,14g二者的混合物的物质的量为0.5mol,含有1mol原子;
B.3mol NO2气体与水完全反应生成硝酸溶液和NO气体,电子转移2mol;
C.标准状况下,11.2LC2H5OH不是气体,物质的量不是0.5mol;
D.计算物质的量n=$\frac{m}{M}$,氨气分子中含有三对共用电子对.
解答 解:A.14gN2与CO组成的混合气体的物质的量为0.5mol,0.5mol混合气体中含有1mol原子,含有的原子数目为NA,故A正确;
B.3NO2+H2O=2HNO3+NO,3mol NO2气体与水完全反应生成硝酸溶液和NO气体,电子转移2mol,1molNO2气体与水完全反应,转移电子数为$\frac{2}{3}$NA,故B错误;
C.标准状况下气体摩尔体积为22.4L/mol,11.2LC2H5OH不是气体,物质的量不是0.5mol,故C错误;
D.常温常压下,17gNH3中物质的量=$\frac{17g}{17g/mol}$=1mol,含有的共用电子对数为3NA,故D错误;
故选A.
点评 本题考查了阿伏伽德罗常数的应用,物质的量和微粒数的计算,氧化还原反应电子转移,气体摩尔体积的应用条件,掌握基础是解题关键,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
7.化学与生活、社会可持续发展密切相关,下列叙述错误的是( )
| A. | CO2的大量排放会导致酸雨的形成 | |
| B. | 黄河三角洲的形成体现了胶体聚沉的性质 | |
| C. | 推广使用燃料电池汽车,可减少颗粒物、CO等有害物质的排放 | |
| D. | 轮船上挂锌锭防止铁腐蚀,属于牺牲阳极的阴极保护法 |
8.食用二氧化硫漂白过的食品,对人体的肝、肾脏等有严重损害.某科研小组设计实验检验二氧化硫的漂白性.回答下列问题:
(一)二氧化硫的制备
实验室一般采用亚硫酸钠与硫酸(浓硫酸与水1:1混合)反应制取二氧化硫:

(1)欲收集一瓶干燥的二氧化硫,选择上图中的装置,其最佳连接顺序为:b→c→d→e→f→g(按气流方向,用小写字母表示).
(二)二氧化硫性质的检验
将上述收集到的SO2通入下列装置中,在一定温度下按图示装置进行实验.
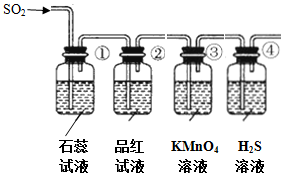
(2)根据上述实验,回答下列问题:
(3)用SO2漂白过的食品中一般残留有亚硫酸盐,科研小组设计了检验食品中是否含有亚硫酸盐的简单方法:将食品剪成碎末放入烧杯,加入适量的水,加热一会儿,冷却至室温,滴加盐酸和试剂A,观察液体的颜色变化既可.
①加热的作用是加快反应速率(或加快食品的溶解),加热时间不能太长的原因是防止亚硫酸盐被氧化.
②试剂A是品红溶液.
(一)二氧化硫的制备
实验室一般采用亚硫酸钠与硫酸(浓硫酸与水1:1混合)反应制取二氧化硫:

(1)欲收集一瓶干燥的二氧化硫,选择上图中的装置,其最佳连接顺序为:b→c→d→e→f→g(按气流方向,用小写字母表示).
(二)二氧化硫性质的检验
将上述收集到的SO2通入下列装置中,在一定温度下按图示装置进行实验.

(2)根据上述实验,回答下列问题:
| 序号 | 实验现象 | 解释原因 |
| ① | 石蕊试液变红 | 石蕊试液变红说明SO2是酸性气体 |
| ② | 品红试液褪色 | SO2具有漂白性 |
| ③ | KMnO4溶液颜色褪色 | 反应的离子方程式5SO2+2H2O+2MnO4-=2Mn2++5SO42-+4H+ |
| ④ | 溶液变浑浊,有黄色沉淀生成 | SO2+2H2S=3S↓+2H2O |
①加热的作用是加快反应速率(或加快食品的溶解),加热时间不能太长的原因是防止亚硫酸盐被氧化.
②试剂A是品红溶液.
12.Q、W、X、Y、Z是原子序数依次增大的短周期元素,Q和Y均满足主族序数与周期序数相等,Q与X、W与Z同主族,Q和W能形成原子个数之比为1:1和2:1的常见化合物.下列说法正确的是( )
| A. | 原子半径:Z>Y>X>W>Q | |
| B. | Q、X形成的化合物的电子式为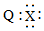 | |
| C. | 最简单氢化物的稳定性:Z>W | |
| D. | 工业上常用电解的方法制备X、Y的单质 |
2.实验室制备硝基苯时,经过配制混酸、硝化反应(50~60℃)、洗涤分液、干燥蒸馏等步骤,下列图示装置和原理能达到实验目的是( )
| A. | 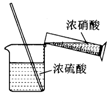 配制混酸 | B. | 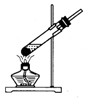 硝化反应 | C. |  分离硝基苯 | D. | 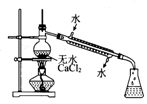 蒸馏硝基苯 |
9.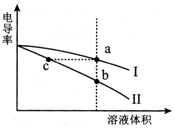 电导率是衡量电解质溶液导电能力大小的物理量.常温下,将相同体积的氢氧化钠溶液和醋酸溶液分别加水稀释,溶液的电导率随溶液体积变化的曲线如图所示.下列说法正确的是( )
电导率是衡量电解质溶液导电能力大小的物理量.常温下,将相同体积的氢氧化钠溶液和醋酸溶液分别加水稀释,溶液的电导率随溶液体积变化的曲线如图所示.下列说法正确的是( )
 电导率是衡量电解质溶液导电能力大小的物理量.常温下,将相同体积的氢氧化钠溶液和醋酸溶液分别加水稀释,溶液的电导率随溶液体积变化的曲线如图所示.下列说法正确的是( )
电导率是衡量电解质溶液导电能力大小的物理量.常温下,将相同体积的氢氧化钠溶液和醋酸溶液分别加水稀释,溶液的电导率随溶液体积变化的曲线如图所示.下列说法正确的是( )| A. | I表示NaOH溶液加水稀释过程中溶液电导率的变化 | |
| B. | a、b、c三点溶液的pH:b>c>a | |
| C. | 将a、b两点溶液混合,所得溶液中:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) | |
| D. | a点水电离出的n(H+)等于c点水电离出的n(H+) |
15.已知X、Y、Z、W为短周期主族元素,在周期表中的相对位置如图,有下列说法:
①若HmXOn为强酸,则X的氢化物溶于水一定显酸性(m、n均为正整数)
②若四种元素均为金属,则Z的最高价氧化物对应的水化物一定为强碱
③若四种元素均为非金属,则W的最高价氧化物对应的水化物一定为强酸
④若四种元素只有一定为金属,则Z与Y的最高价氧化物对应的水化物一定为强酸.
其中不正确的说法有几项( )
①若HmXOn为强酸,则X的氢化物溶于水一定显酸性(m、n均为正整数)
②若四种元素均为金属,则Z的最高价氧化物对应的水化物一定为强碱
③若四种元素均为非金属,则W的最高价氧化物对应的水化物一定为强酸
④若四种元素只有一定为金属,则Z与Y的最高价氧化物对应的水化物一定为强酸.
其中不正确的说法有几项( )
| X | Y |
| Z | W |
| A. | 1项 | B. | 2项 | C. | 3项 | D. | 4项 |
16.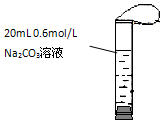 如图,将2mL浓度为6mol/L的盐酸用注射器通过橡皮塞慢慢注入,玻璃管中出现小气泡,气泡在溶液中逐渐上升的过程中消失.对该反应过程的推断不合理的是:( )
如图,将2mL浓度为6mol/L的盐酸用注射器通过橡皮塞慢慢注入,玻璃管中出现小气泡,气泡在溶液中逐渐上升的过程中消失.对该反应过程的推断不合理的是:( )
 如图,将2mL浓度为6mol/L的盐酸用注射器通过橡皮塞慢慢注入,玻璃管中出现小气泡,气泡在溶液中逐渐上升的过程中消失.对该反应过程的推断不合理的是:( )
如图,将2mL浓度为6mol/L的盐酸用注射器通过橡皮塞慢慢注入,玻璃管中出现小气泡,气泡在溶液中逐渐上升的过程中消失.对该反应过程的推断不合理的是:( )| A. | 有反应CO32-+2H+→CO2↑+H2O | |
| B. | 有反应CO32-+H+→HCO3-发生 | |
| C. | 有反应CO32-+CO2+H2O→2HCO3-发生 | |
| D. | 加快盐酸注入速度不会改变反应现象 |
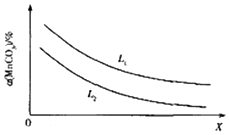 MnO2是常见的氧化剂、催化剂和活性电极材料.
MnO2是常见的氧化剂、催化剂和活性电极材料.