题目内容
15.已知X、Y、Z、W为短周期主族元素,在周期表中的相对位置如图,有下列说法:①若HmXOn为强酸,则X的氢化物溶于水一定显酸性(m、n均为正整数)
②若四种元素均为金属,则Z的最高价氧化物对应的水化物一定为强碱
③若四种元素均为非金属,则W的最高价氧化物对应的水化物一定为强酸
④若四种元素只有一定为金属,则Z与Y的最高价氧化物对应的水化物一定为强酸.
其中不正确的说法有几项( )
| X | Y |
| Z | W |
| A. | 1项 | B. | 2项 | C. | 3项 | D. | 4项 |
分析 X、Y、Z、W为短周期主族元素,由元素在周期表中的相对位置,可知X、Y处于第二周期,Z、W处于第三周期.
①若HmXOn为强酸,则X为N元素;
②若四种元素均为金属,则X为Li、Z为Na、Y为Be、W为Mg;
③若四种元素均为非金属,X、Z至少处于ⅣA族,W可能为P、S或Cl;
④若四种元素只有一种为金厲,则X为B、Z为Al、Y为C、W为Si.
解答 解:X、Y、Z、W为短周期主族元素,由元素在周期表中的相对位置,可知X、Y处于第二周期,Z、W处于第三周期.
①若HmXOn为强酸,则X为N元素,其氢化物为氨气,水溶液呈碱性,故错误;
②若四种元素均为金属,则X为Li、Z为Na、Y为Be、W为Mg,Z的最高价氧化物对应水化物为NaOH,属于强碱,故正确;
③若四种元素均为非金属,X、Z至少处于ⅣA族,W可能为P、S或Cl,最高价含氧酸中硫酸、高氯酸为强酸,而磷酸属于中强酸,故C错误;
④若四种元素只有一种为金厲,则X为B、Z为Al、Y为C、W为Si,Z、Y 二者的最高价氧化物对应的水化物分别为氢氧化铝、碳酸,二者不是强酸,故错误;
其中不正确的说法有3项;
故选C.
点评 本题考查元素周期表与元素化合物性质的综合应用,侧重考查学生发散思维能力和对基础知识的应用能力,题目难度中等,需要学生熟练掌握元素周期表结构、元素化合物性质.

练习册系列答案
相关题目
16.下列实验操作正确且能达到实验目的是( )
| A. | 在蒸发皿中加热胆矾晶体制无水硫酸铜 | |
| B. | 用向下排空气法收集 NO2 气体 | |
| C. | 用 K3[Fe(CN)6]溶液检验 FeCl2 溶液中的 Fe2+ | |
| D. | 将 CO2 与 HCl 混合气体通过碱石灰可得到纯净的 CO2 |
17.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 常温常压下,14g由N2与CO组成的混合气体含有的原子数目为NA | |
| B. | 常温常压下,1molNO2气体与水完全反应,转移电子数为NA | |
| C. | 标准状况下,11.2LC2H5OH中所含的分子数为0.5NA | |
| D. | 常温常压下,17gNH3中含有的共用电子对数为4NA |
3.某同学采用硫铁矿焙烧取硫后的烧渣(主要成分为Fe2O3、SiO2、Al2O3,不考虑其他杂质)制取七水合硫酸亚铁(FeSO4•7H2O),设计了如图流程:下列说法不正确的是( )
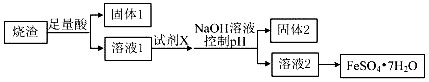

| A. | 溶解烧渣选用足量硫酸,试剂X选用铁粉 | |
| B. | 固体1中一定含有SiO2,控制pH是为了使Al3+转化为Al(OH)3,进入固体2 | |
| C. | 从溶液2得到FeSO4•7H2O产品的过程中,须控制条件防止其氧化和分解 | |
| D. | 若改变方案,在溶液1中直接加NaOH至过量,得到的沉淀用硫酸溶解,其溶液经结晶分离也可得到FeSO4•7H2O |
10.化学与生产、生活密切相关,下列事实的解释正确的是 ( )
| 选项 | 事实 | 解释 |
| A | 酸雨的pH<5.6 | CO2溶解在雨水中 |
| B | 稻草、甘蔗渣可用来造纸 | 稻草、甘蔗渣富含纤维素 |
| C | 化石燃料燃烧时采取固硫措施 | 提高化石燃料的利用率 |
| D | 将水中的铁闸门连接电源的负极而防腐 | 利用牺牲阳极的阴极保护法 |
| A. | A | B. | B | C. | C | D. | D |
7.下列有关Cl、N、S等非金属元素化合物的说法正确的是( )
| A. | 漂白粉是纯净物,其成分就是次氯酸钙 | |
| B. | 实验室可用浓硫酸干燥氨气 | |
| C. | 实验室可用NaOH溶液处理SO2和HCl废气 | |
| D. | 浓盐酸、浓硫酸、浓硝酸都有强氧化性,能氧化金属铜 |
4.下列现象或应用不能用胶体的知识解释的是( )
| A. | 肾功能衰竭等疾病引起的血液中毒,可利用血液透析进行治疗 | |
| B. | 氯化钙溶液中加入碳酸钠溶液会出现白色沉淀 | |
| C. | 水泥、冶金工厂常用高压电除去工厂烟尘,减少对空气的污染 | |
| D. | 江河入海口形成三角州 |