题目内容
17. 298K时,在FeCl3溶液中加少量锌粒后,Fe3+被还原成Fe2+.据此某学习小组设计如图所示的原电池装置.下列有关说法正确的是( )
298K时,在FeCl3溶液中加少量锌粒后,Fe3+被还原成Fe2+.据此某学习小组设计如图所示的原电池装置.下列有关说法正确的是( )| A. | 正极电极反应为Zn-2e-═Zn2+ | |
| B. | 左边烧杯中溶液的红色变浅 | |
| C. | Pt电极上有气泡出现 | |
| D. | 该电池的总反应为:3Zn+2Fe3+═3Zn2++2 Fe |
分析 Zn失去电子发生氧化反应,为负极反应,Fe3+在正极得电子被还原为Fe2+,以此解答.
解答 解:A.Zn失去电子发生氧化反应,为负极反应,故A错误;
B.Fe3+在正极得电子被还原为Fe2+,溶液红色褪去,故B正确;
C.铂电极上Fe3+被还原为Fe2+,没有气体生成,故C错误;
D.该电池总反应为:Zn+2Fe3+═2Fe2++Zn2+,没有单质生成,故D错误.
故选B.
点评 本题考查原电池知识,侧重于原电池的设计,注意把握电解方程式的书写以及原电池的工作原理,难度不大.

练习册系列答案
相关题目
7.在实验室中,对下列实验事故或药品的处理正确的是( )
| A. | 金属钠着火燃烧时,用干燥沙土灭火 | |
| B. | 点燃可燃性气体前,都必须先检验气体的纯度 | |
| C. | 少量浓硫酸沾在皮肤上,立即用氢氧化钠溶液擦洗 | |
| D. | 配制H2SO4溶液时,先在量筒中加一定体积的水,再在搅拌下慢慢加入浓H2SO4 |
 某温度时,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示.由图中所给数据进行分析:
某温度时,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示.由图中所给数据进行分析: ═CH-CHO
═CH-CHO +CO$→_{氢化铝}^{HCl}$
+CO$→_{氢化铝}^{HCl}$

 +CH3CHO$\stackrel{稀碱}{→}$
+CH3CHO$\stackrel{稀碱}{→}$ .
.
 $→_{反应条件1}^{G}$H$\stackrel{浓硫酸}{→}$
$→_{反应条件1}^{G}$H$\stackrel{浓硫酸}{→}$ 试剂G的结构简式是CH3CH2CHO.
试剂G的结构简式是CH3CH2CHO. 和
和 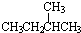 ②
② 和
和 
 与
与