题目内容
9.下列各化合物中(填入编号)(1)属于同系物的是①③
(2)属于同位素的是⑤⑥
(3)属于同素异形体的是④⑧
(4)属于同分异构体的是②⑦
(5)属于同种物质的是⑨⑩
①
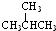 和
和  ②
②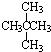 和
和 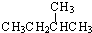
③CH4和CH3CH2CH3;④白磷、红磷:⑤H、D、T;⑥35Cl 与 37Cl
⑦乙醇(CH3CH2OH)和甲醚(CH3OCH3);⑧C60 与C70 ⑨苏打和纯碱⑩
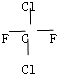 与
与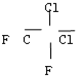
分析 (1)同系物:结构相似,在分子组成上相差一个或若干个CH2原子团的化合物;
(2)同位素:质子数相同中子数不同的同一元素的原子互称同位素;
(3)同素异形体:同种元素组成的不同单质;
(4)同分异构体:分子式相同结构不同的化合物;
(5)同种物质指组成和结构都相同的物质.
解答 解:(1)①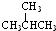 和
和  ③CH4和CH3CH2CH3;结构相似,都属于烷烃,分子组成相差1个或多个CH2原子团,互为同系物,故答案为:①③;
③CH4和CH3CH2CH3;结构相似,都属于烷烃,分子组成相差1个或多个CH2原子团,互为同系物,故答案为:①③;
(2)⑤H、D、T;⑥35Cl 与 37Cl质子数相同,中子数不同,互为同位素,故答案为:⑤⑥;
(3)④白磷、红磷⑧C60 与C70 是同种元素组成的结构不同的单质,互为同素异形体,故答案为:④⑧;
(4)② 和
和 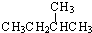 ⑦乙醇(CH3CH2OH)和甲醚(CH3OCH3)分子式相同,结构不同,为同分异构体,故答案为:②⑦;
⑦乙醇(CH3CH2OH)和甲醚(CH3OCH3)分子式相同,结构不同,为同分异构体,故答案为:②⑦;
(5)⑨苏打是纯碱的俗名、⑩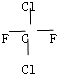 与
与 组成和结构都相同,为同一物质,故答案为:⑨⑩.
组成和结构都相同,为同一物质,故答案为:⑨⑩.
点评 本题主要考查了同系物、同分异构体、同位素、同素异形体、同一物质的区别,难度不大,注意把握概念的内涵与外延.

练习册系列答案
相关题目
19.在实验室里可用如图1所示装置制取氯酸钾、次氯酸钠并探究氯水的性质.
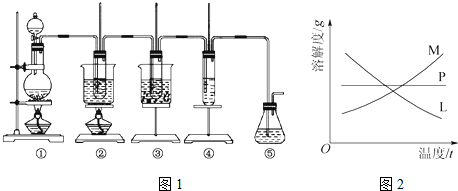
图中:①为氯气发生装置;②的试管里盛有15mL 30%KOH溶液,并置于热水浴中;③的试管里盛有15mL8%NaOH溶液,并置于冰水浴中;④的试管里加有紫色石蕊试液;⑤为尾气吸收装置.
请填写下列空白:
(1)制取氯气时,在烧瓶里加入一定量的二氧化锰,通过分液漏斗(填写仪器名称)向烧瓶中加入适量的浓盐酸.实验时为了除去氯气中的氯化氢气体,可在①与②之间安装盛有B(填字母)的净化装置.
A.碱石灰 B.饱和食盐水
C.浓硫酸 D.饱和碳酸氢钠溶液
(2)比较制取氯酸钾和次氯酸钠的条件,二者的差异是碱溶液(或反应物)的浓度不同,反应温度不同.
反应完毕经冷却后,②的试管中有大量晶体析出.图2中符合该晶体溶解度曲线的是M(填字母);从②的试管中分离出该晶体的方法是过滤(填实验操作名称).
(3)本实验中制取次氯酸钠的离子方程式是Cl2+2OH-═ClO-+Cl-+H2O.
(4)实验中可观察到④的试管里溶液的颜色发生了如下变化,请填写下表中的空白:

图中:①为氯气发生装置;②的试管里盛有15mL 30%KOH溶液,并置于热水浴中;③的试管里盛有15mL8%NaOH溶液,并置于冰水浴中;④的试管里加有紫色石蕊试液;⑤为尾气吸收装置.
请填写下列空白:
(1)制取氯气时,在烧瓶里加入一定量的二氧化锰,通过分液漏斗(填写仪器名称)向烧瓶中加入适量的浓盐酸.实验时为了除去氯气中的氯化氢气体,可在①与②之间安装盛有B(填字母)的净化装置.
A.碱石灰 B.饱和食盐水
C.浓硫酸 D.饱和碳酸氢钠溶液
(2)比较制取氯酸钾和次氯酸钠的条件,二者的差异是碱溶液(或反应物)的浓度不同,反应温度不同.
反应完毕经冷却后,②的试管中有大量晶体析出.图2中符合该晶体溶解度曲线的是M(填字母);从②的试管中分离出该晶体的方法是过滤(填实验操作名称).
(3)本实验中制取次氯酸钠的离子方程式是Cl2+2OH-═ClO-+Cl-+H2O.
(4)实验中可观察到④的试管里溶液的颜色发生了如下变化,请填写下表中的空白:
| 实验现象 | 原因 |
| 溶液逐渐变为红色 | 氯气与水反应生成的H+使石蕊变色 |
| 随后溶液逐渐变为无色 | 氯气与水反应生成的HClO将石蕊氧化为无色物质 |
| 然后溶液从无色逐渐变为黄绿色 | 继续通入的氯气溶于水使溶液呈黄绿色 |
17.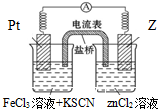 298K时,在FeCl3溶液中加少量锌粒后,Fe3+被还原成Fe2+.据此某学习小组设计如图所示的原电池装置.下列有关说法正确的是( )
298K时,在FeCl3溶液中加少量锌粒后,Fe3+被还原成Fe2+.据此某学习小组设计如图所示的原电池装置.下列有关说法正确的是( )
 298K时,在FeCl3溶液中加少量锌粒后,Fe3+被还原成Fe2+.据此某学习小组设计如图所示的原电池装置.下列有关说法正确的是( )
298K时,在FeCl3溶液中加少量锌粒后,Fe3+被还原成Fe2+.据此某学习小组设计如图所示的原电池装置.下列有关说法正确的是( )| A. | 正极电极反应为Zn-2e-═Zn2+ | |
| B. | 左边烧杯中溶液的红色变浅 | |
| C. | Pt电极上有气泡出现 | |
| D. | 该电池的总反应为:3Zn+2Fe3+═3Zn2++2 Fe |
4.下列叙述正确的是( )
| A. | 含1molNa2S的溶液,最多可吸收2molSO2 | |
| B. | 可以用浓硫酸除去镀在铝表面的铜镀层 | |
| C. | Li、C、S分别在足量氧气中燃烧均生成一种相应氧化物 | |
| D. | NaHCO3、Na2CO3、(NH4)2CO3三种固体受热后均能生成气体 |
14.如图是对物质的一种分类方法,该分类法的名称及序号①~⑥代表的物质可以是( )
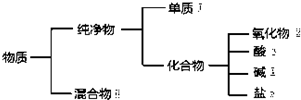

| A. | 交叉分类法 ①硫磺 ②氯水 ④小苏打 ⑥青铜 | |
| B. | 树状分类法 ①白磷 ④纯碱 ⑤水玻璃 ⑥水泥 | |
| C. | 交叉分类法 ②硅石 ③氢氟酸 ⑤纯碱 ⑥漂白粉 | |
| D. | 树状分类法 ②冰水 ④烧碱 ⑤胆矾 ⑥氨水 |
1.决定化学反应速率快慢的主要因素是( )
| A. | 温度 | B. | 浓度 | C. | 催化剂 | D. | 反应物的性质 |
19.用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,22.4L CCl4中含有的分子数为NA | |
| B. | 常温下,23g Na完全被氧化失去的电子数为NA | |
| C. | 标准状况下,22.4L CH4中含有的电子数为NA | |
| D. | 0.3mol•L-1AlCl3溶液中含有的氯离子数为0.9NA |
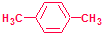 ,该烃在光照下生成的一氯代物在PMR谱中可能产生的各组信号峰的峰面积之比为3:2:2:2.
,该烃在光照下生成的一氯代物在PMR谱中可能产生的各组信号峰的峰面积之比为3:2:2:2. 现有A、B两种金属分别与盐酸反应,产生氢气的速率相近.请设计一个原电池实验证明A、B两种金属的活动性?(电极材料:A、B,电解质溶液:盐酸,其它实验用品可自选),请在方框中画出简易装置图.如A是较不活泼的金属,则A的现象是有气泡逸出,那么,B即是活泼的金属.
现有A、B两种金属分别与盐酸反应,产生氢气的速率相近.请设计一个原电池实验证明A、B两种金属的活动性?(电极材料:A、B,电解质溶液:盐酸,其它实验用品可自选),请在方框中画出简易装置图.如A是较不活泼的金属,则A的现象是有气泡逸出,那么,B即是活泼的金属.