题目内容
下列几种元素的表达式错误的是( )
A、F-的电子排布图: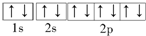 |
B、Na+的结构示意图: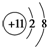 |
| C、Mg2+的电子排布式:1s22s22p6 |
| D、Cr的简化电子排布式:[Ar]3d44s2 |
考点:原子核外电子排布,原子结构示意图
专题:原子组成与结构专题
分析:A、氟离子的核电荷数为9,核外电子数为9+1=10,核外电子排布式为1s2 2s22p6;
B、Na+的原子核内有11个质子,核外有10个电子,结构示意图为 ;
;
C、Mg2+的含有的电子数为12-2=10,核外电子排布式为1s2 2s22p6;
D、Cr的3d能级上有5个原子轨道,达到半满时能量较低.
B、Na+的原子核内有11个质子,核外有10个电子,结构示意图为
 ;
;C、Mg2+的含有的电子数为12-2=10,核外电子排布式为1s2 2s22p6;
D、Cr的3d能级上有5个原子轨道,达到半满时能量较低.
解答:
解:A、氟离子的核电荷数为9,核外电子数为9+1=10,核外电子排布式为1s2 2s22p6,电子排布图: ,故A正确;
,故A正确;
B、Na+的原子核内有11个质子,核外有10个电子,结构示意图为 ,故B正确;
,故B正确;
C、Mg2+的含有的电子数为12-2=10,核外电子排布式为1s2 2s22p6,故C正确;
D、Cr的3d能级上有5个原子轨道,达到半满时能量较低,因此简化电子排布式:[Ar]3d54s1,故D错误;
故选D.
 ,故A正确;
,故A正确;B、Na+的原子核内有11个质子,核外有10个电子,结构示意图为
 ,故B正确;
,故B正确;C、Mg2+的含有的电子数为12-2=10,核外电子排布式为1s2 2s22p6,故C正确;
D、Cr的3d能级上有5个原子轨道,达到半满时能量较低,因此简化电子排布式:[Ar]3d54s1,故D错误;
故选D.
点评:本题考查原子核外电子排布,为高考常见题型,难度不大,注意把握原子核外电子的排布规律,把握电子排布式和轨道式的书写方法.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列说法错误的是( )
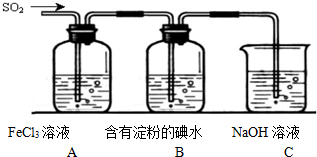
| A、向某溶液加入盐酸酸化的BaCl2溶液,若生成白色沉淀,则原溶液中一定含有SO42 |
| B、向某溶液中加入2滴KSCN溶液,溶液不显红色,再向溶液中滴几滴新制的氯水,溶液变为红色,该溶液中一定含有Fe2+ |
| C、向FeSO4溶液中加入NaOH,可以看到先出现白色沉淀,迅速变为灰绿色,最终变成红褐色 |
| D、不能用澄清的石灰水来鉴别Na2CO3和NaHCO3溶液 |
下列各项叙述中,正确的是( )
| A、镁原子由1s22s22p63s2→1s22s22p63p2时,原子释放能量,由基态转化成激发态 |
| B、同一原子中,2p,3p,4p能级的轨道依次增多 |
| C、所有原子任一能层的s电子云轮廓图都是球形,但球的半径大小不同 |
| D、CH2O和ClO4-的中心原子上都含有孤对电子 |
下列分子中所有原子都满足最外层8电子结构的是( )
| A、光气(COCl2) |
| B、五氯化磷(PCl5) |
| C、氟利昂(CF2Cl2) |
| D、三氟化硼(BF3) |
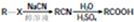
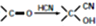
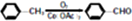
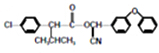 )
)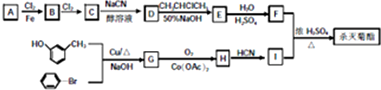
 注:合成路线的书写格式参照如下示例流程图:
注:合成路线的书写格式参照如下示例流程图:
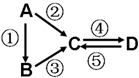 A、B、C、D均为中学化学常见的纯净物,A是单质.它们之间有如下的反应关系:
A、B、C、D均为中学化学常见的纯净物,A是单质.它们之间有如下的反应关系: