题目内容
为探究SO2气体还原Fe3+、I2,使用的药品和装置如图所示:
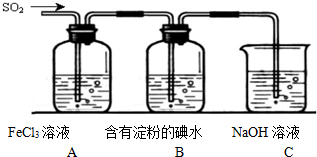
(1)SO2与FeCl3溶液反应的离子方程式是: ;装置C的作用是 .
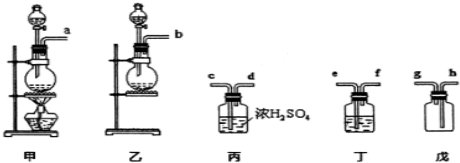
(2)若要从A中所得溶液提取晶体,必须进行的实验操作步骤:蒸发浓缩、冷却结晶、 、洗涤、自然干燥,在这一系列操作中没有用到的仪器有 (填序号).
A.蒸发皿 B.石棉网 C.漏斗 D.烧杯 E.玻璃棒 F.坩埚
(3)在上述装置中通入过量的SO2,为了验证A中SO2与Fe3+发生了氧化还原反应,他们取A中的溶液,分成三份,并设计了如下实验:
方案①:往第一份试液中加入KMnO4溶液,紫红色褪去
方案②:往第二份试液加入KSCN溶液,不变红,再加入新制的氯水,溶液变红
方案③:往第三份试液加入用稀盐酸酸化的BaCl2,产生白色沉淀.
上述方案不合理的是 原因是 .
(4)能表明I-的还原性弱于SO2的现象是 .

(1)SO2与FeCl3溶液反应的离子方程式是:
(2)若要从A中所得溶液提取晶体,必须进行的实验操作步骤:蒸发浓缩、冷却结晶、
A.蒸发皿 B.石棉网 C.漏斗 D.烧杯 E.玻璃棒 F.坩埚
(3)在上述装置中通入过量的SO2,为了验证A中SO2与Fe3+发生了氧化还原反应,他们取A中的溶液,分成三份,并设计了如下实验:
方案①:往第一份试液中加入KMnO4溶液,紫红色褪去
方案②:往第二份试液加入KSCN溶液,不变红,再加入新制的氯水,溶液变红
方案③:往第三份试液加入用稀盐酸酸化的BaCl2,产生白色沉淀.
上述方案不合理的是
(4)能表明I-的还原性弱于SO2的现象是
考点:探究二氧化硫与水和品红溶液的反应
专题:实验设计题
分析:(1)三价铁离子具有氧化性,二氧化硫具有还原性,二者能够发生氧化还原反应生成亚铁离子和硫酸;二氧化硫有毒,不能直接排放到空气中,为酸性氧化物能够与氢氧化钠反应生成亚硫酸钠和水;
(2)从A中所得溶液提取晶体为绿矾,溶液中得到绿矾的实验操作是蒸发浓缩,冷却结晶,过滤洗涤,干燥步骤得到;
(3)二氧化硫、Fe2+具有还原性,和氧化剂能发生氧化还原反应,能使高锰酸钾溶液褪色现象明显;
(4)B中发生SO2+I2+2H2O=2HI+H2SO4,还原剂的还原性大于还原产物.
(2)从A中所得溶液提取晶体为绿矾,溶液中得到绿矾的实验操作是蒸发浓缩,冷却结晶,过滤洗涤,干燥步骤得到;
(3)二氧化硫、Fe2+具有还原性,和氧化剂能发生氧化还原反应,能使高锰酸钾溶液褪色现象明显;
(4)B中发生SO2+I2+2H2O=2HI+H2SO4,还原剂的还原性大于还原产物.
解答:
解:(1)铁离子能够氧化二氧化硫,SO2与FeCl3溶液反应的离子方程式为:SO2+2Fe3++2H2O=2Fe2++SO42-+4H+,二氧化硫有毒,不能直接排放到空气中,二氧化硫酸性氧化物能够与氢氧化钠反应生成亚硫酸钠和水,所以可以用氢氧化钠溶液吸收二氧化硫,反应的化学方程式为:2NaOH+SO2=Na2SO3+H2O,
故答案为:2H2O+SO2+2Fe3+═SO42-+4H++2Fe2+;吸收SO2尾气,防止污染空气;
(2)溶液中得到绿矾的实验操作是蒸发浓缩,冷却结晶,过滤洗涤,干燥步骤得到,所以在这一系列操作中没有用到的仪器有石棉网、坩埚,
故答案为:过滤;B、F;
(3)二氧化硫有还原性,高锰酸钾有强氧化性,二氧化硫能与高锰酸钾发生氧化还原反应使高锰酸钾溶液褪色,Fe2+也使高锰酸钾溶液褪色,所以上述方案中不合理的是①,
故答案为:①;因为A的溶液中含有SO2,SO2也能使KMnO4溶液褪色;
(4)B中发生SO2+I2+2H2O=2HI+H2SO4,还原剂的还原性大于还原产物的还原性,则I-的还原性弱于SO2,现象为紫色变为无色,故答案为:B中蓝色溶液褪色.
故答案为:2H2O+SO2+2Fe3+═SO42-+4H++2Fe2+;吸收SO2尾气,防止污染空气;
(2)溶液中得到绿矾的实验操作是蒸发浓缩,冷却结晶,过滤洗涤,干燥步骤得到,所以在这一系列操作中没有用到的仪器有石棉网、坩埚,
故答案为:过滤;B、F;
(3)二氧化硫有还原性,高锰酸钾有强氧化性,二氧化硫能与高锰酸钾发生氧化还原反应使高锰酸钾溶液褪色,Fe2+也使高锰酸钾溶液褪色,所以上述方案中不合理的是①,
故答案为:①;因为A的溶液中含有SO2,SO2也能使KMnO4溶液褪色;
(4)B中发生SO2+I2+2H2O=2HI+H2SO4,还原剂的还原性大于还原产物的还原性,则I-的还原性弱于SO2,现象为紫色变为无色,故答案为:B中蓝色溶液褪色.
点评:本题考查物质制备实验及性质实验,题目难度中等,明确各装置的作用及发生的化学反应是解答本题的关键,注意掌握二氧化硫的性质及检验方法.

练习册系列答案
 导学教程高中新课标系列答案
导学教程高中新课标系列答案 小学课时特训系列答案
小学课时特训系列答案
相关题目
下列几种元素的表达式错误的是( )
A、F-的电子排布图: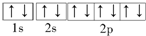 |
B、Na+的结构示意图: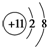 |
| C、Mg2+的电子排布式:1s22s22p6 |
| D、Cr的简化电子排布式:[Ar]3d44s2 |
下列说法正确的是( )
| A、一定温度下,某溶液的pH<7,则该溶液呈酸性 |
| B、在水中加入少量碳酸钠固体将抑制水的电离 |
| C、0.02mol?L-1CH3COOH溶液和0.01mol?L-1NaOH溶液等体积混合,则溶液中:2c(H+)+c(CH3COOH)=2 c(OH-)+c(CH3COO-) |
| D、浓度均为0.1mol/L的NH4Cl溶液和NH4HSO4溶液,前者的c(NH4+)大于后者 |
 25℃时,在25mL0.1mol/L的氢氧化钠溶液中,逐滴加入0.2mol/LCH3COOH,溶液的pH的变化曲线如图所示,下列分析的结论正确的是( )
25℃时,在25mL0.1mol/L的氢氧化钠溶液中,逐滴加入0.2mol/LCH3COOH,溶液的pH的变化曲线如图所示,下列分析的结论正确的是( )| A、若B点的横坐标a=12.5,且有c(Na+)=c(CH3COO-) |
| B、对曲线上A、B间任何一点,溶液中都有:c(Na+)>c(OH-)>c(CH3COO-)>c(H+) |
| C、D点时,c(CH3COO-)+c(CH3COOH)=c(Na+) |
| D、C点时,c(CH3COO-)=c(Na+)>c(H+)=c(OH-) |
常温下,下列叙述不正确的是( )
| A、在醋酸溶液的pH=a,将此溶液稀释1倍后,溶液的pH=b,则a<b |
| B、在滴有酚酞溶液的氨水里,加入NH4Cl至溶液恰好无色,则此时溶液的pH<7 |
| C、1.0×10-3mol/L盐酸的pH=3.0,1.0×10-8mol/L盐酸的pH<8.0 |
| D、若1mLpH=1的盐酸与100mLNaOH溶液混合后,溶液的pH=7则NaOH溶液的pH=11 |
近几年一种新型的甜味剂--木糖醇悄悄的走进人们的生活,因为木糖醇是一种理想的蔗糖代替品,它具有甜味足、溶解性好、防龋齿、适合糖尿病患者等优点.木糖醇是一种白色粉末状的固体,结构简式为:CH2OH(CHOH)3CH2OH.下列有关木糖醇的叙述错误的是( )
| A、木糖醇与葡萄糖、果糖等一样是一种单糖 |
| B、木糖醇极易溶于水 |
| C、木糖醇是一种五元醇 |
| D、木糖醇是一种无糖型植物甜味剂 |
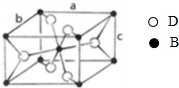 ,该氧化物的化学式为
,该氧化物的化学式为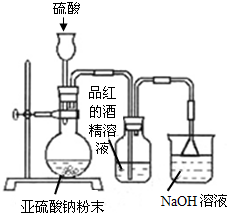 某研究性学习小组在研究二氧化硫漂白作用时,从“氯气的漂白作用实际上是氯气与水反应生成的次氯酸的漂白作用”得到启发.为了探究二氧化硫漂白作用到底是二氧化硫本身还是二氧化硫与水作用的产物,该小组设计了如下实验.请回答相关问题.
某研究性学习小组在研究二氧化硫漂白作用时,从“氯气的漂白作用实际上是氯气与水反应生成的次氯酸的漂白作用”得到启发.为了探究二氧化硫漂白作用到底是二氧化硫本身还是二氧化硫与水作用的产物,该小组设计了如下实验.请回答相关问题.