题目内容
20.有如下反应:KMnO4+C+H2SO4→MnSO4+K2SO4+CO2↑+H2O(1)配平上面的方程式,在横线上填入系数.
(2)在方程式上标出电子转移的方向和数目.
(3)如反应后得到了1molCO2,则在反应中有0.8molMn原子被还原(选“氧化”或“还原”),它得到(选“失去”或“得到”)了4NA个电子.
分析 (1)根据氧化还原反应中得失电子数相等和原子守恒来配平化学方程式;
(2)高锰酸钾中锰元素化合价降低7-2=5价,碳元素化合价升高4-0=4价,化合价升高数=化合价降低数,所以高锰酸钾前的系数是4,碳单质前的系数是5,所以生成5mol的二氧化碳转移20mol电子,由此分析解答;
(3)反应转移20mol电子生成了二氧化碳5mol,所以得到了1molCO2,则反应中有0.8molMn原子被还原,得到4NA个电子.
解答 解:(1)高锰酸钾中锰元素化合价降低7-2=5价,碳元素化合价升高4-0=4价,化合价升高数=化合价降低数,所以高锰酸钾前的系数是4,碳单质前的系数是5,根据原子守恒,二氧化碳前是5,硫酸锰前是4,硫酸钾前面是2,根据硫酸跟守恒,所以硫酸前面是6,据氧原子和氢原子守恒,产物少6个水分子,故答案为:5;4;6;5;4;2;6H2O;
(2)高锰酸钾中锰元素化合价降低7-2=5价,碳元素化合价升高4-0=4价,化合价升高数=化合价降低数,所以高锰酸钾前的系数是4,碳单质前的系数是5,所以生成5mol的二氧化碳转移20mol电子, ,故答案为:
,故答案为: ;
;
(3)反应转移20mol电子生成了二氧化碳5mol,所以得到了1molCO2,则反应中有0.8molMn原子被还原,得到4NA个电子,故答案为:0.8;还原;得到;4NA.
点评 本题考查学生氧化还原反应中的有关概念以及转移电子的知识,可以根据所学知识进行回答,难度不大.

练习册系列答案
相关题目
8.CO2和氢氧化钠溶液反应,所得产物中Na2CO3和NaHCO3物质的量之比为3:5,则参加反应的CO2和NaOH的物质的量之比为( )
| A. | 3:5 | B. | 1:2 | C. | 8:11 | D. | 18:8 |
15.下列仪器名称正确的是( )
| A. |  钥匙 | B. |  蒸发皿 | C. |  镊子 | D. |  滴瓶 |
5.下列说法正确的是( )
| A. | 胆矾(CuSO4•5H2O)是混合物 | |
| B. | 加热胆矾失去结晶水的过程是风化 | |
| C. | 氯化钙易吸水而发生潮解,所以可作干燥剂 | |
| D. | 从饱和溶液中析出的晶体都含有结晶水 |
10.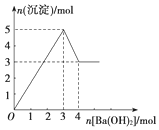 如图表示向某溶液中滴加Ba(OH)2溶液时,沉淀的物质的量随Ba(OH)2的物质的量的变化关系.该溶液的成分可能是( )
如图表示向某溶液中滴加Ba(OH)2溶液时,沉淀的物质的量随Ba(OH)2的物质的量的变化关系.该溶液的成分可能是( )
 如图表示向某溶液中滴加Ba(OH)2溶液时,沉淀的物质的量随Ba(OH)2的物质的量的变化关系.该溶液的成分可能是( )
如图表示向某溶液中滴加Ba(OH)2溶液时,沉淀的物质的量随Ba(OH)2的物质的量的变化关系.该溶液的成分可能是( )| A. | MgSO4 | B. | Al2(SO4)3 | C. | FeSO4 | D. | NaAlO2 |