题目内容
12.2molN2在标准状况下的体积是44.8L;N2的摩尔质量是28g/mol;同温同压下,相同体积的O3和N2所含的分子数相同(填“相同”或“不相同”);将4gNaOH固体溶于水配制成250mL溶液,此溶液中NaOH的物质的量浓度 为0.4mol/L.分析 根据V=nVm来计算体积;摩尔质量在数值上等于相对分子质量;同温同压下,相同体积的O3和N2的物质的量相等,根据N和n的关系来回答;根据c=$\frac{n}{V}$来计算物质的量浓度.
解答 解:2molN2在标准状况下的体积V=2mol×22.4L/mol=44.8;N2的摩尔质量是28g/mol;同温同压下,相同体积的O3和N2物质的量相等,所含的分子数相同;将4gNaOH固体溶于水配制成250mL溶液,此溶液中NaOH的物质的量浓度是$\frac{\frac{4g}{40g/mol}}{0.25L}$=0.4mol/L.
故答案为:44.8;28g/mol;相同;0.4mol/L.
点评 本题考查常用化学计量的有关计算,比较基础,注意对公式的理解与灵活运用.

练习册系列答案
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案
相关题目
1.设NA为阿伏伽德罗常数的值,下列说法中正确的是( )
| A. | 2.4g金属镁所含电子数目为0.2NA | |
| B. | 7.8gNa2O2中含有阴离子数目为0.2NA | |
| C. | 71g氯气溶于水配成溶液,所得溶液中含Cl-数目为1 NA | |
| D. | 4℃,18g水所含分子数目为NA |
3.向a mL0.25mol•L-1的AlCl3溶液中加入金属钠,反应完全后,恰好只形成NaCl和NaAlO2的混合溶液,则加入金属钠的物质的量为( )
| A. | 2.5a×10-4mol | B. | a×10-3mol | C. | 7.5a×10-4mol | D. | a×10-4mol |
7.室温下,下列有关电解质溶液的叙述正确的是( )
| A. | 同浓度、同体积的强酸与强碱溶液混合后,溶液的pH=7 | |
| B. | pH=10的Ba(OH)2溶液和pH=13的NaOH溶液等体积混合后pH=10.7(已知1g2=0.3) | |
| C. | 将10mLpH=a的盐酸与100mLpH=b的Ba(OH)2溶液混合后恰好中和,则a+b=13 | |
| D. | pH=2的盐酸与pH=12的氨水等体积混合后所得溶液显中性 |
17.由苯和乙醛组成的混合液体,经测定其中碳的质量分数为72%,则混合物中氧元素的质量分数为( )
| A. | 2.14% | B. | 19.56% | C. | 22.65% | D. | 32.00% |
4.用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 2.4g镁变成Mg2+时失去的电子数目为0.2NA | |
| B. | 常温常压下,11.2L氧气所含的O原子数为NA | |
| C. | 如果11.2LN2中含有n个分子,则阿伏加德罗常数一定为2n | |
| D. | 1 mol•L-1的KSCN和1mol•L-1KAl(SO4)2溶液中,所含K+数都是NA |
1.下列关于金属钠的叙述中,说法正确的是( )
| A. | 钠在空气中燃烧,发出黄色火焰 | |
| B. | 钠在空气中燃烧,产物是Na2O | |
| C. | 钠是银白色金属,硬度大,熔点高 | |
| D. | 取用金属钠时,剩余的钠不能放回原瓶 |
2.下列有关化学用语表示正确的是( )
| A. | H2O2的电子式: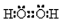 | |
| B. | 次氯酸分子的结构式:H-Cl-O | |
| C. | 乙醇的分子式:C2H5OH | |
| D. | 1,1-二溴乙烷的结构简式:CH3CHBr2 |