题目内容
9.氢能是发展中的新能源,它的利用包括氢的制备、储存和应用三个环节.回答下列问题:(1)与汽油相比,氢气作为燃料的优点是污染小、可再生、来源广、资源丰富、燃烧热值高氢气直接燃烧的能量
转换率远低于燃料电池,写出碱性氢氧燃料电池的负极反应式:H2+2OH--2e-=2H2O.
(2)利用太阳能直接分解水制氢,是最具吸引力的制氢途径,其能量转化形式为将光能转化为化学能
(3)化工生产的副产氢也是氢气的来源.电解法制取有广泛用途的Na2FeO4,同时获得氢气:Fe+2H2O+2OH-$\frac{\underline{\;通电\;}}{\;}$FeO42-+3H2,工作原理如图1所示.若氢氧化钠溶液浓度过高,铁电极区会产生红褐色物质.已知:Na2FeO4只在强碱性条件下稳定,易被H2还原.
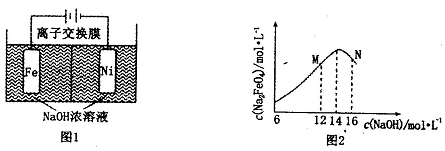
①电解过程中,阳极电极反应式:Fe-6e-+8OH-=FeO42-+4H2O
②c(Na2FeO4)随初始c(NaOH)的变化如图2,任选M、N两点中的一点,分析c(Na2FeO4)低于最高值的原因:M点:c(OH-)低,Na2FeO4稳定性差,且反应慢(或N点:c(OH-)过高,铁电极上有氢氧化铁生成,使Na2FeO4产率降低).
分析 (1)与汽油相比,氢气作为燃料的优点有污染小、可再生、来源广、资源丰富、燃烧热值高等;碱性氢氧燃料电池的负极反应式为H2+2OH--2e-=2H2O;
(2)利用太阳能直接分解水制氢,是将光能转化为化学能;
(3)①阳极发生氧化反应,铁失电子生成高铁酸根离子;
②根据题意Na2FeO4只在强碱性条件下稳定,在M点,c(OH-)低,Na2FeO4稳定性差,且反应慢,在N点:c(OH-)过高,铁电极上有氢氧化铁生成,使Na2FeO4产率降低.
解答 解:(1)与汽油相比,氢气作为燃料的优点有污染小、可再生、来源广、资源丰富、燃烧热值高等;碱性氢氧燃料电池的负极反应式为H2+2OH--2e-=2H2O,
故答案为:污染小、可再生、来源广、资源丰富、燃烧热值高;H2+2OH--2e-=2H2O;
(2)利用太阳能直接分解水制氢,是将光能转化为化学能,
故答案为:将光能转化为化学能;
(3)①阳极发生氧化反应,铁失电子生成高铁酸根离子,电极反应式为:Fe-6e-+8OH-=FeO42-+4H2O,故答案为:Fe-6e-+8OH-=FeO42-+4H2O;
②根据题意Na2FeO4只在强碱性条件下稳定,在M点,c(OH-)低,Na2FeO4稳定性差,且反应慢,在N点:c(OH-)过高,铁电极上有氢氧化铁生成,使Na2FeO4产率降低,
故答案为:M点:c(OH-)低,Na2FeO4稳定性差,且反应慢(或N点:c(OH-)过高,铁电极上有氢氧化铁生成,使Na2FeO4产率降低).
点评 本题考查电解池原理,明确各个电极上发生的反应是解本题关键,注意阳极发生的反应,题目难度中等.

练习册系列答案
 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案
相关题目
20.下列说法正确的是( )
| A. | 苯的同系物都能使酸性高锰酸钾溶液褪色 | |
| B. | 红外光谱、核磁共振氢谱都可以鉴别乙醇和甲醚 | |
| C. | 符合相同通式的不同物质一定是同系物 | |
| D. | 某有机物燃烧后只生成二氧化碳和水,则一定不含有氧元素 |
17.设NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A. | 将1 mol BaCl2 溶于水所形成的溶液中含NA个氯离子 | |
| B. | 2克氢气所含原子数约为6.02×1023 | |
| C. | 标准状况下,22.4 L SO2所含的分子数为NA | |
| D. | 常温常压下,22.4 L O2和O3的混合气体所含分子数为2NA |
4.下列说法正确的是( )
| A. | 在Na2CO3、NaHCO3两溶液中,离子种类不相同 | |
| B. | 在等体积、等物质的量浓度的Na2CO3、NaHCO两溶液中,阳离子总数相等 | |
| C. | 在Na2CO3溶液中一定有c(Na+)+c(H+)=c(HCO3-)+c(OH-)+2c(CO32-) | |
| D. | 在Na2CO3溶液中一定有c(Na+)>c(CO32-)>c(H+)>c(OH-) |
14.下列物质溶于水能导电,但不属于电解质的是( )
| A. | 过氧化钠 | B. | 蔗糖 | C. | 氯气 | D. | 氯化铁 |
1.设NA为阿伏伽德罗常数的值,下列说法中正确的是( )
| A. | 2.4g金属镁所含电子数目为0.2NA | |
| B. | 7.8gNa2O2中含有阴离子数目为0.2NA | |
| C. | 71g氯气溶于水配成溶液,所得溶液中含Cl-数目为1 NA | |
| D. | 4℃,18g水所含分子数目为NA |
 .
.