题目内容
科学家近年来研制出一种新型细菌燃料电池,利用细菌将有机物转化为甲烷,然后将甲烷通入以KOH为电解质的燃料电池发电.电池负极反应为( )
| A、CH4-8e-+8OH-=CO2+6H2O |
| B、O2+4H++4e-=2H2O |
| C、CH4+10OH--8e-=C32-+7H2O |
| D、O2+2H2O+4e-=4OH- |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:碱性甲烷燃料电池工作时,通入甲烷的一极为原电池的负极,发生氧化反应,电极反应式为CH4+10OH--8e-=CO32-+7H2O,通入氧气的一极为电池的正极,发生还原反应,电极方程式为O2+2H2O+4e-=4OH-,以此解答该题.
解答:
解:甲烷中C元素的化合价为-4价,具有还原性,则碱性甲烷燃料电池工作时,通入甲烷的一极为原电池的负极,发生氧化反应,电极反应式为CH4+10OH--8e-=CO32-+7H2O,通入氧气的一极为电池的正极,发生还原反应,电极方程式为O2+2H2O+4e-=4OH-,
故选C.
故选C.
点评:本题考查燃料电池知识,侧重于电极方程式的书写,答题时注意判断电池的正负极反应,把握电极方程式的书写方法,此为该类题目考查的重点,学习中注意积累该部分知识.

练习册系列答案
相关题目
由环已烷制取1,3-环已二烯,需经过的顺序( )
| A、取代-加成-消去-氧化 |
| B、取代-消去-加成-消去 |
| C、取代-取代-消去-加成 |
| D、氧化-取代-消去-加成 |
下列各组物质按酸、碱、盐、电解质分类顺次排列的是( )
| A、硫酸,纯碱,明矾,二氧化硫 |
| B、盐酸,熟石灰,苛性钠,石灰水 |
| C、冰醋酸,乙醇,碳酸钠,氨水 |
| D、硝酸,烧碱,碳酸钙,氯化钠 |
下列说法错误的是( )
| A、0.1 mol?L-1的醋酸中加入水或加入冰醋酸均可使平衡向电离方向移动 |
| B、等pH的醋酸和碳酸,分别加水稀释后溶液的pH仍相等,则醋酸中加入水的体积少 |
| C、等物质的量浓度的CH3COONa和Na2CO3溶液,后者溶液中水的电离程度大 |
| D、常温下10ml 0.02 mol?L-1HCl溶液与10ml 0.02 mol?L-1Ba(OH)2溶液充分混合,若混合后溶液的体积为20ml,则溶液的pH=10 |
下列有关说法正确的是( )
| A、常温下Ksp(Ag2CrO4)=1.1×10-12,Ksp(AgCl)=1.8×10-10,则Ag2CrO4的溶解度小于AgCl |
| B、纯碱溶于热水中,去油污效果增强,说明纯碱的水解是放热反应 |
| C、为保护海轮的船壳,常在船壳上镶入锌块 |
| D、以熔融Al2O3为电解质进行电解冶炼铝,熔融体中Al3+向阳极移动 |
现有常温下的四份溶液:①pH=2的CH3COOH溶液;②pH=2的稀HCl;③0.01mol/L氨水;④0.01mol/L NaOH溶液.下列说法正确的是( )
| A、四份溶液中水的电离程度由大到小的顺序为:①=②=④<③ |
| B、若将②、③等体积混合,则混合液的pH为7 |
| C、将四份溶液稀释相同倍数后,溶液的pH:③>④>②>① |
| D、若在10mL①中加入④至pH刚好等于7,则C(Na+)=C(CH3COO-),混合溶液总体积<20mL(假设混和溶液体积为酸和碱溶液体积之和) |
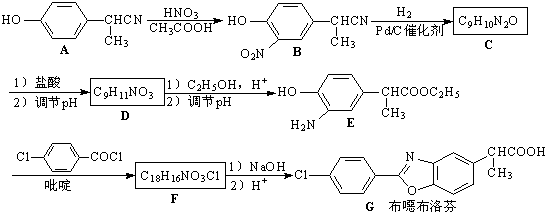

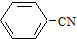 为原料制备
为原料制备 的合成路线流程图(无机试剂任选).合成路线流程图示例如图:CH2=CH2
的合成路线流程图(无机试剂任选).合成路线流程图示例如图:CH2=CH2 化学学科中的化学平衡、电离平衡、水解平衡和溶解平衡均符合勒夏特列原理.请回答下列问题:
化学学科中的化学平衡、电离平衡、水解平衡和溶解平衡均符合勒夏特列原理.请回答下列问题: