题目内容
在隔绝空气的条件下,某同学将一块质量为5g,部分被氧化的钠块用一张已用针刺一些小孔且打磨过的光亮铝箔包好,然后放入盛有水的水槽中.待钠块反应完全后,此时 测得铝箔质量比反应前减少了0.54g,水槽中溶液的总体积为2.0L,且溶液中NaOH的浓
度为0.090mol?L-1
(1)写出该实验中发生反应的化学方程式.
(2)试通过计算确定该钠块中钠元素的质量分数.
度为0.090mol?L-1
(1)写出该实验中发生反应的化学方程式.
(2)试通过计算确定该钠块中钠元素的质量分数.
考点:化学方程式的有关计算
专题:计算题
分析:(1)部分被氧化的钠用除去氧化膜并用针刺一些小孔的铝箔包好放入水中,氧化钠与水反应生成氢氧化钠,钠与水反应生成氢氧化钠与氢气,铝与氢氧化钠溶液反应生成偏铝酸钠与氢气;
(2)反应的有关方程式为:Na2O+H2O=2NaOH,2Na+2H2O=2NaOH+H2↑,2Al+2NaOH+2H2O=2NaAlO2+3H2↑,根据铝的质量可计算出铝与NaOH反应消耗氢氧化钠的物质的量,和反应后溶液中氢氧化钠的量,根据Na元素质量守恒的角度列式解答.
(2)反应的有关方程式为:Na2O+H2O=2NaOH,2Na+2H2O=2NaOH+H2↑,2Al+2NaOH+2H2O=2NaAlO2+3H2↑,根据铝的质量可计算出铝与NaOH反应消耗氢氧化钠的物质的量,和反应后溶液中氢氧化钠的量,根据Na元素质量守恒的角度列式解答.
解答:
解:(1)部分被氧化的钠用除去氧化膜并用针刺一些小孔的铝箔包好放入水中,氧化钠与水反应生成氢氧化钠,钠与水反应生成氢氧化钠与氢气,铝与氢氧化钠溶液反应生成偏铝酸钠与氢气,反应方程式为:Na2O+H2O=2NaOH,2Na+2H2O=2NaOH+H2↑,2Al+2NaOH+2H2O=2NaAlO2+3H2↑,
答:实验中发生反应的化学方程式为2Na+2H2O=2NaOH+H2↑、Na2O+H2O=2NaOH、2Al+2NaOH+2H2O=2NaAlO2+3H2↑;
(2)n(Al)=0.54g/27g?mol-1=0.020mol
根据反应2Al+2NaOH+2H2O=2NaAlO2+3H2↑可得由铝消耗NaOH的物质的量为n(NaOH)=0.020mol
又因为反应后溶液中的NaOH的物质的量为n(NaOH)=2.0L×0.090mo1?L-1=0.180mol
所以溶液中Na+的总物质的量即原金属钠的总物质的量为n(Na+)=0.180mol+0.020mol=0.2mol
该钠块中钠元素的质量分数为:0.2mol×23 g?mol-1=4.6g,所以钠块中钠元素的质量分数:
×100%=92%,
答:该钠块中钠元素的质量分数约为92%.
答:实验中发生反应的化学方程式为2Na+2H2O=2NaOH+H2↑、Na2O+H2O=2NaOH、2Al+2NaOH+2H2O=2NaAlO2+3H2↑;
(2)n(Al)=0.54g/27g?mol-1=0.020mol
根据反应2Al+2NaOH+2H2O=2NaAlO2+3H2↑可得由铝消耗NaOH的物质的量为n(NaOH)=0.020mol
又因为反应后溶液中的NaOH的物质的量为n(NaOH)=2.0L×0.090mo1?L-1=0.180mol
所以溶液中Na+的总物质的量即原金属钠的总物质的量为n(Na+)=0.180mol+0.020mol=0.2mol
该钠块中钠元素的质量分数为:0.2mol×23 g?mol-1=4.6g,所以钠块中钠元素的质量分数:
| 4.6g |
| 5g |
答:该钠块中钠元素的质量分数约为92%.
点评:本题考查钠的性质以及混合物的计算等,过程比较复杂,解题时注意从守恒的角度计算,可以利用方程式计算,题目难度中等.

练习册系列答案
相关题目
科学家发现了某种元素的一种新原子,其质量是a g,12C原子的质量是b g,NA是阿伏加德罗常数的值,下列说法不正确的是( )
A、由已知信息可得NA=
| ||
B、W g该原子的物质的量一定是
| ||
C、W g该原子中含有
| ||
| D、该元素的摩尔质量是aNA g?mol-1 |
现有常温下的四种溶液(如下表):
下列有关叙述中正确的是( )
| ① | ② | ③ | ④ | |
| 溶液 | 氨水 | 氢氧化钠溶液 | 醋酸 | 盐酸 |
| pH | 11 | 11 | 3 | 3 |
| A、分别加水稀释10倍,四种溶液的pH:②>①>④>③ |
| B、将③、④分别稀释到pH=5,由水电离出氢离子的浓度均减小100倍 |
| C、在①、②中分别加入适量的氯化铵晶体后,①的pH减小,②的pH不变 |
| D、将①、④两种溶液等体积混合,所得溶液中:c(OH-):c(H+)>1 |
科学家近年来研制出一种新型细菌燃料电池,利用细菌将有机物转化为甲烷,然后将甲烷通入以KOH为电解质的燃料电池发电.电池负极反应为( )
| A、CH4-8e-+8OH-=CO2+6H2O |
| B、O2+4H++4e-=2H2O |
| C、CH4+10OH--8e-=C32-+7H2O |
| D、O2+2H2O+4e-=4OH- |
下列元素性质的递变规律正确的是( )
| A、第一电离能:B<Be<Mg<Na |
| B、元素的电负性:O>N>S>P |
| C、气态氢化物的稳定性:NH3<CH4<PH3<SiH4 |
| D、原子半径:Be<B<C<N |
已知:KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O.如下图所示,将少量试剂分别放入培养皿中的相应位置,实验时将浓盐酸滴在KClO3晶体上,并用表面皿盖好.下列选项中由实验现象得出的结论完全正确的是( )
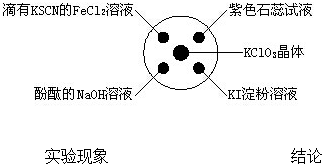

| A、滴有KSCN的FeCl2溶液变红色Cl2具有还原性 |
| B、滴有酚酞的NaOH溶液褪色 Cl2具有酸性 |
| C、石蕊溶液先变为红色后褪色Cl2具有漂白性 |
| D、KI淀粉溶液中变蓝色 Cl2具有氧化性 |