��Ŀ����
��¯������ұ��������Ҫ��������������Ҫ��ӦΪ��Fe2O3��s��+3CO��g��?2Fe��s��+3CO2��g����H=-28.5kJ?��mol-1
��1����֪��C��ʯī��+CO2 ��g��?2CO��g����H=+172.5kJ?mol-1��Ӧ��Fe2O3 ��S��+3C��ʯī��?2Fe��s��+3CO��g����H= kJ?mol-1
��2��ұ������Ӧ Fe2O3��s��+3CO��g��?2Fe��s��+3CO2��g����H=-28.5kJ?mol-1
��ƽ�ⳣ������ʽK= ���¶Ƚ��ͺ�Kֵ ��������������䡱��С������
��3����T��Cʱ���÷�Ӧ��ƽ�ⳣ��K=27����1L�����ܱ����������У��ֱ��±���ʾ�������ʣ���Ӧ����һ��ʱ���ﵽƽ�⣮
�ټ�������CO��ƽ��ת����Ϊ
������˵����ȷ���� ������ĸ����
a����������CO��ƽ��ת����С�ڼ�����
b���ס��������У�CO2��ƽ��Ũ��֮��Ϊ2��3
c��������������ѹǿ���ֲ���ʱ����־��Ӧ�ﵽƽ��״̬
d���������������ܶȱ��ֲ���ʱ����־��Ӧ�ﵽƽ��״̬
��4��������ҵ�ǹ��ҹ�ҵ�Ļ�������ش������ʴ����������е��й����⣮
��ͼ1�ĸ�װ�ÿɷ�ֹ��������ʴ �����ţ���
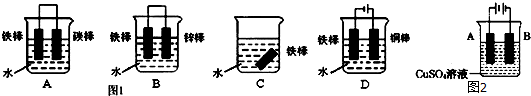
����ʵ�������У����������ı����ͭ��ֹ������ʴ��װ��ʾ��ͼ��ͼ2��A�缫��Ӧ�Ľ����� ��дԪ�����ƣ���B�缫�ĵ缫��Ӧʽ�� ��
�۶Ʋ������ͭ���ȶ�п�������ױ���ʴ�����Ҫ˵��ԭ�� ��
��1����֪��C��ʯī��+CO2 ��g��?2CO��g����H=+172.5kJ?mol-1��Ӧ��Fe2O3 ��S��+3C��ʯī��?2Fe��s��+3CO��g����H=
��2��ұ������Ӧ Fe2O3��s��+3CO��g��?2Fe��s��+3CO2��g����H=-28.5kJ?mol-1
��ƽ�ⳣ������ʽK=
��3����T��Cʱ���÷�Ӧ��ƽ�ⳣ��K=27����1L�����ܱ����������У��ֱ��±���ʾ�������ʣ���Ӧ����һ��ʱ���ﵽƽ�⣮
| Fe2 O3 | CO | Fe | CO2 | |
| ������ | 1.0mol | 1.0mol | 1.0mol | 1.0mol |
| ������ | 1.0mol | 2.0mol | 1.0mol | 1.0mol |
������˵����ȷ����
a����������CO��ƽ��ת����С�ڼ�����
b���ס��������У�CO2��ƽ��Ũ��֮��Ϊ2��3
c��������������ѹǿ���ֲ���ʱ����־��Ӧ�ﵽƽ��״̬
d���������������ܶȱ��ֲ���ʱ����־��Ӧ�ﵽƽ��״̬
��4��������ҵ�ǹ��ҹ�ҵ�Ļ�������ش������ʴ����������е��й����⣮
��ͼ1�ĸ�װ�ÿɷ�ֹ��������ʴ

����ʵ�������У����������ı����ͭ��ֹ������ʴ��װ��ʾ��ͼ��ͼ2��A�缫��Ӧ�Ľ�����
�۶Ʋ������ͭ���ȶ�п�������ױ���ʴ�����Ҫ˵��ԭ��
���㣺�йط�Ӧ�ȵļ���,�����ĵ绯ѧ��ʴ�����,��ѧƽ���Ӱ������,��ѧƽ��״̬���ж�
ר�⣺
��������1�������Ȼ�ѧ����ʽ�����ݸ�˹���ɹ���Ŀ���Ȼ�ѧ����ʽ���㷴Ӧ�ȣ�
��2��ƽ�ⳣ�������������Ũ��ϵ������֮�����Է�Ӧ��Ũ��ϵ������֮���������¶ȶ�ƽ���ƶ���Ӱ���ж��¶ȶ�ƽ�ⳣ����Ӱ�죻
��3����Ũ����Qc=1��С��ƽ�ⳣ������Ӧ������Ӧ���У���ƽ��ʱ�μӷ�Ӧ��COΪxmol����������ʽ��ʾ��ƽ��ʱ����ֵ����ʵ���������ƽ�ⳣ���з��̼��㣬�ڽ��ת���ʶ�����㣻
��a�����ݳ�ʼ����������K��ֵ�������ʽ������������CO��ƽ��ת���ʣ�Ȼ����ױȽϣ�
b������a������ݷ������ɽ��
c����Ӧǰ�����������ȣ���Ӧǰ��ѹǿ���䣻
d������CO���ܶ���CO2���ܶȲ�ͬ������
��4������ԭ������������ӵ�Դ����������������
�ڵ��ʱ�����ʱ���Ʋ������������Ƽ����ӵ�Դ�������Ʋ����������Ƽ����������������Һ�к��жƲ����Ԫ�أ������Ϸ���������Ӧ�������Ϸ�����ԭ��Ӧ��
�۵�����Ϊԭ��ظ���ʱ�������绯ѧ��ʴ��
��2��ƽ�ⳣ�������������Ũ��ϵ������֮�����Է�Ӧ��Ũ��ϵ������֮���������¶ȶ�ƽ���ƶ���Ӱ���ж��¶ȶ�ƽ�ⳣ����Ӱ�죻
��3����Ũ����Qc=1��С��ƽ�ⳣ������Ӧ������Ӧ���У���ƽ��ʱ�μӷ�Ӧ��COΪxmol����������ʽ��ʾ��ƽ��ʱ����ֵ����ʵ���������ƽ�ⳣ���з��̼��㣬�ڽ��ת���ʶ�����㣻
��a�����ݳ�ʼ����������K��ֵ�������ʽ������������CO��ƽ��ת���ʣ�Ȼ����ױȽϣ�
b������a������ݷ������ɽ��
c����Ӧǰ�����������ȣ���Ӧǰ��ѹǿ���䣻
d������CO���ܶ���CO2���ܶȲ�ͬ������
��4������ԭ������������ӵ�Դ����������������
�ڵ��ʱ�����ʱ���Ʋ������������Ƽ����ӵ�Դ�������Ʋ����������Ƽ����������������Һ�к��жƲ����Ԫ�أ������Ϸ���������Ӧ�������Ϸ�����ԭ��Ӧ��
�۵�����Ϊԭ��ظ���ʱ�������绯ѧ��ʴ��
���
�⣺��1����֪����Fe2O3��s��+3CO��g��?2Fe��s��+3CO2��g����H=-28.5kJ?mol-1
��C��ʯī��+CO2 ��g��?2CO��g����H=+172.5kJ?mol-1��
���ݸ�˹���ɣ���+�ڡ�3��Fe2O3 ��S��+3C��ʯī��?2Fe��s��+3CO��g��
�ʡ�H=��-28.5kJ?mol-1��+��+172.5kJ?mol-1����3=+489kJ?mol-1��
�ʴ�Ϊ��489��
��2��Fe2O3��s��+3CO��g��?2Fe��s��+3CO2��g����H=-28.5kJ?mol-1��ƽ�ⳣ������ʽK=
���÷�Ӧ�Ƿ��ȷ�Ӧ�������¶�ƽ��������У�ƽ�ⳣ������
�ʴ�Ϊ��
������
��3������T��ʱ���÷�Ӧ��ƽ�ⳣ��K=27����������Ũ����Qc=1��С��ƽ�ⳣ������Ӧ������Ӧ���У�������һ����̼���ʵ���Ϊx����
Fe2O3��s��+3CO��g��?2Fe��s��+3CO2��g��
��ʼ����mol����1 1
�仯����mol����x x
ƽ������mol����1-x 1+x
��Ӧǰ������������䣬���������ʵ�������Ũ�ȼ���ƽ�ⳣ������
=27��x=0.5����CO��ת����=
��100%=50%��
�ʴ�Ϊ��50%��
��a����T��ʱ���÷�Ӧ��ƽ�ⳣ��K=27����������Ũ����Qc=
=
��С��ƽ�ⳣ������Ӧ������Ӧ���У�������һ����̼���ʵ���Ϊy����
Fe2O3��s��+3CO��g��?2Fe��s��+3CO2��g��
��ʼ����mol����2 1
�仯����mol����y y
ƽ������mol����2-y 1+y
��Ӧǰ������������䣬���������ʵ�������Ũ�ȼ���ƽ�ⳣ������
=27��x=1.25����CO��ת����=
��100%=62.5%��50%����������CO��ƽ��ת���ʴ��ڼ���������a����
b���ס��������У�CO2��ƽ��Ũ�ȷֱ�Ϊ��1+x=1.5mol��1+y=1+1.25=2.25mol��ƽ��Ũ��֮��Ϊ2��3����b��ȷ��
c���÷�ӦΪ�����������ķ�Ӧ������������ѹǿʼ�ղ��䣬������ѹǿ�ж�ƽ��״̬����c����
d��CO���ܶ���CO2���ܶȲ�ͬ�����Ե������ڵ��ܶȲ���ʱ������ƽ��״̬����d��ȷ��
�ʴ�Ϊ��b��d��
��4������ԭ������������ӵ�Դ������������������ԭ��ظ��������ӵ�Դ�����������ٱ���ʴ��
��ѡBD��
�ڵ��ʱ���Ʋ������������Ƽ����ӵ�Դ�����������϶�ͭ��ͭ��������������������A��ͭ��B������B��ͭ���ӵõ��ӷ�����ԭ��Ӧ���缫��ӦʽΪCu2++2e-=Cu��
�ʴ�Ϊ��ͭ��Cu2++2e-=Cu��
��п������ͭ�������������μ���������ͭ���ã��γ�ԭ��ط�Ӧʱ����Ϊ������ͭΪ��������п�������ã��γ�ԭ��ط�Ӧʱ����Ϊ������пΪ�����������Ա��������Ʋ������ͭ���ȶ�п�������ױ���ʴ��
�ʴ�Ϊ��п������ͭ�������������μ������Ʋ�������ڳ�ʪ�������γ�ԭ��أ���п����Ϊ�����ܵ�����������ͭ���������������ױ���ʴ��
��C��ʯī��+CO2 ��g��?2CO��g����H=+172.5kJ?mol-1��
���ݸ�˹���ɣ���+�ڡ�3��Fe2O3 ��S��+3C��ʯī��?2Fe��s��+3CO��g��
�ʡ�H=��-28.5kJ?mol-1��+��+172.5kJ?mol-1����3=+489kJ?mol-1��
�ʴ�Ϊ��489��
��2��Fe2O3��s��+3CO��g��?2Fe��s��+3CO2��g����H=-28.5kJ?mol-1��ƽ�ⳣ������ʽK=
| c3(co2) |
| c3(co) |
�ʴ�Ϊ��
| c3(co2) |
| c3(co) |
��3������T��ʱ���÷�Ӧ��ƽ�ⳣ��K=27����������Ũ����Qc=1��С��ƽ�ⳣ������Ӧ������Ӧ���У�������һ����̼���ʵ���Ϊx����
Fe2O3��s��+3CO��g��?2Fe��s��+3CO2��g��
��ʼ����mol����1 1
�仯����mol����x x
ƽ������mol����1-x 1+x
��Ӧǰ������������䣬���������ʵ�������Ũ�ȼ���ƽ�ⳣ������
| (1+x)3 |
| (1-x)3 |
| 0.5mol |
| 1mol |
�ʴ�Ϊ��50%��
��a����T��ʱ���÷�Ӧ��ƽ�ⳣ��K=27����������Ũ����Qc=
| 1 |
| 23 |
| 1 |
| 8 |
Fe2O3��s��+3CO��g��?2Fe��s��+3CO2��g��
��ʼ����mol����2 1
�仯����mol����y y
ƽ������mol����2-y 1+y
��Ӧǰ������������䣬���������ʵ�������Ũ�ȼ���ƽ�ⳣ������
| (1+y)3 |
| (2-y)3 |
| 1.25 |
| 2 |
b���ס��������У�CO2��ƽ��Ũ�ȷֱ�Ϊ��1+x=1.5mol��1+y=1+1.25=2.25mol��ƽ��Ũ��֮��Ϊ2��3����b��ȷ��
c���÷�ӦΪ�����������ķ�Ӧ������������ѹǿʼ�ղ��䣬������ѹǿ�ж�ƽ��״̬����c����
d��CO���ܶ���CO2���ܶȲ�ͬ�����Ե������ڵ��ܶȲ���ʱ������ƽ��״̬����d��ȷ��
�ʴ�Ϊ��b��d��
��4������ԭ������������ӵ�Դ������������������ԭ��ظ��������ӵ�Դ�����������ٱ���ʴ��
��ѡBD��
�ڵ��ʱ���Ʋ������������Ƽ����ӵ�Դ�����������϶�ͭ��ͭ��������������������A��ͭ��B������B��ͭ���ӵõ��ӷ�����ԭ��Ӧ���缫��ӦʽΪCu2++2e-=Cu��
�ʴ�Ϊ��ͭ��Cu2++2e-=Cu��
��п������ͭ�������������μ���������ͭ���ã��γ�ԭ��ط�Ӧʱ����Ϊ������ͭΪ��������п�������ã��γ�ԭ��ط�Ӧʱ����Ϊ������пΪ�����������Ա��������Ʋ������ͭ���ȶ�п�������ױ���ʴ��
�ʴ�Ϊ��п������ͭ�������������μ������Ʋ�������ڳ�ʪ�������γ�ԭ��أ���п����Ϊ�����ܵ�����������ͭ���������������ױ���ʴ��
���������⿼�����Ȼ�ѧ����ʽ��˹���ɼ���Ӧ�ã�ƽ�ⳣ������Ӧ�ã���ѧƽ������ʽ��ʽ���㷽����ԭ���֪ʶ�ȣ�Ϊ��Ƶ���㣬ע�����ԭ��صĹ���ԭ���Լ������ķ���������ע�⻯ѧƽ������ʽ��ʽ���㣬��Ŀ�Ѷ��еȣ�

��ϰ��ϵ�д�
 ��У����ϵ�д�
��У����ϵ�д�
�����Ŀ
���и�����������ȷ���ǣ�������
A��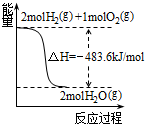 �ɵ�H2��ȼ����Ϊ483.6kJ?mol-1 |
B��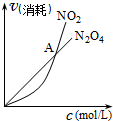 ��ʾ���º��������·����Ŀ��淴Ӧ2NO2��g���TN2O4��g���������ʵ�Ũ��������������֮��Ĺ�ϵ�����н���A��Ӧ��״̬Ϊ��ѧƽ��״̬ |
C��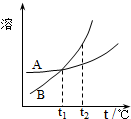 ��ʾA��B�����ʵ��ܽ�����¶ȵı仯�������t1��ʱ��A��B������Һ�ֱ�������t2��ʱ�����ʵ���������B��A |
D��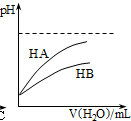 ��ʾ�����£�ϡ��HA��HB�������ϡ��Һʱ����ҺpH�����ˮ���ı仯������ʱͬŨ�ȵ�NaA��Һ��pHС��NaB��Һ |
Ŀǰ��ˮ���������Ҫ����֮һ�ǿ������������գ�������ͼ���£������ƶϲ��������ǣ�������


| A���ȿ����ܴ��������������ӷ������� |
| B��SO2������ķ�Ӧ����ʽ��SO2+2H2O+Br2��H2SO4+2HBr |
| C��������ѭ�����õ�������SO2��Br2��Cl2�ȶ��� |
| D��û�в���ֱ�������庣ˮ�õ����������Ҫԭ����Ϊ�˽��� |
�ڽ���θ����ʱ�����˷��á����͡�����Ҫ�ɷ������ᱵ����25��ʱ��1Lˮ��Լ���ܽ�2.33��10-3g���ᱵ����25��ʱ���ᱵ��Ksp= ��
�����й�˵����ȷ���ǣ�������
A����-CH3�� ��-OH��-COOH����ԭ������������γɵ��л����У�����������ʵ���4�� ��-OH��-COOH����ԭ������������γɵ��л����У�����������ʵ���4�� | ||
B��ij���˷ܼ��Ľṹ��ʽ��ͼ ��1mol��������Ũ��ˮ��Ӧʱ�������Br2Ϊ6mol ��1mol��������Ũ��ˮ��Ӧʱ�������Br2Ϊ6mol | ||
C���л���X��Y��M��ת����ϵΪ�����ۡ�X��Y
| ||
D���߷��ӻ����� ��������Ϊ�Ա���������Ҷ��� ��������Ϊ�Ա���������Ҷ��� |