题目内容
在进行胃部透视时,病人服用“钡餐”的主要成分是硫酸钡.在25℃时,1L水中约能溶解2.33×10-3g硫酸钡,则25℃时硫酸钡的Ksp= .
考点:难溶电解质的溶解平衡及沉淀转化的本质
专题:电离平衡与溶液的pH专题
分析:n(BaSO4)=
=10-5mol,在25℃时,1L水中约能溶解2.33×10-3g硫酸钡,则c(Ba2+)=c(SO42-)=10-5mol/L,结合Ksp=c(Ba2+)×c(SO42-)计算.
| 2.33×10-3g |
| 233g/mol |
解答:
解:n(BaSO4)=
=10-5mol,在25℃时,1L水中约能溶解2.33×10-3g硫酸钡,则c(Ba2+)=c(SO42-)=10-5mol/L,
则25℃时硫酸钡的Ksp=c(Ba2+)×c(SO42-)=10-5×10-5=10-10,
故答案为:10-10.
| 2.33×10-3g |
| 233g/mol |
则25℃时硫酸钡的Ksp=c(Ba2+)×c(SO42-)=10-5×10-5=10-10,
故答案为:10-10.
点评:本题考查难溶电解质知识,为高频考点,侧重于学生的分析、计算能力的考查,注意相关计算公式的运用,难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
稀溶液一般有依数性,即在一定温度下,相同体积的溶液中溶质粒子数目越多,蒸气压下降数值越大.浓度均为0.1mol?L-1的下列稀溶液,其蒸气压最小的是( )
| A、H2SO3溶液 |
| B、C6H12O6溶液 |
| C、NaCl溶液 |
| D、NH3?H2O溶液 |
用黄铁矿可以制取H2SO4,再用H2SO4可以制取化肥(NH4)2SO4.煅烧含FeS280.2%的黄铁矿75.0t,最终生产出79.2t(NH4)2SO4.已知NH3的利用率为92.6%,H2SO4的利用率为89.8%,试求黄铁矿制取H2SO4时的损失率为( )
| A、23.8% |
| B、33.4% |
| C、35.6% |
| D、63.8% |
实验室中不同的试剂有不同的保存方法,下列保存方法中不正确的是 ( )
| A、保存硫酸亚铁溶液需加入铁钉和少量硫酸 |
| B、金属钠保存在装有煤油的玻璃塞广口瓶中 |
| C、溴化银固体保存在棕色玻璃塞的广口瓶中 |
| D、保存浓硝酸需用带橡皮塞子的棕色细口瓶 |
0.1mol?L-1的稀盐酸与0.2mol?L-1醋酸钠溶液等体积完全反应后,测得反应后的溶液中c(CH3COO-)>c(Cl-),则下列判断中错误的是( )
| A、温度为298K时,pH<7 |
| B、c(CH3COOH)+c(CH3COO-)=0.1 mol?L-1 |
| C、c(CH3COOH)<c(CH3COO-) |
| D、c(CH3COO-)+c(OH-)=c(Na+)+c(H+) |
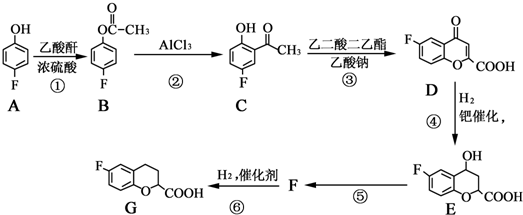
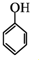 和乙酸酐为原料制备
和乙酸酐为原料制备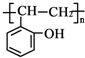 的合成路
的合成路