题目内容
2.科学家发现用二氧化钛(TiO2)作催化剂可以使水在光照条件下分解制得廉价的氢气,这使氢能源的研究和应用更向前迈进了一步.下列说法正确的是( )| A. | 使用二氧化钛作催化剂使水快速分解的同时放出大量热 | |
| B. | 该过程涉及到的反应为氧化还原反应 | |
| C. | 该反应的原理是:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2+O2 | |
| D. | 每产生氢气44.8L,转移电子数目为2NA |
分析 A.水分解是吸热反应;
B.存在化合价的变化的反应是氧化还原反应;
C.该反应的原理是:2H2O$\frac{\underline{\;TiO_{2}\;}}{光照}$2H2↑+O2↑;
D.状况不知,无法由体积求物质的量.
解答 解:A.催化剂的使用未改变反应的热效应,而水分解是吸热反应,故A错误;
B.存在化合价的变化的反应是氧化还原反应,该反应中H、O元素的化合价发生变化,故B正确;
C.二氧化钛(TiO2)作催化剂可以使水在光照条件下分解制得廉价的氢气,该反应的原理是:2H2O$\frac{\underline{\;TiO_{2}\;}}{光照}$2H2↑+O2↑,故C错误;
D.状况不知,无法由体积求物质的量,所以转移电子数目不知,故D错误;
故选B.
点评 本题考查了氧化还原反应、化学反应中的能量变化、气体摩尔体积的应用、以及方程式的书写,题目综合性强,但比较容易,侧重于考查学生对基础知识的应用能力.

练习册系列答案
相关题目
13.1mol某金属与含3mol HNO3的稀硝酸恰好完全反应,则该金属可能是( )
| A. | Fe | B. | Al | C. | Cu | D. | Ag |
7.将下列物质分别加到湿的红色布条上,不能使其褪色是( )
| A. | 新制氯水 | B. | 液氯 | ||
| C. | 次氯酸钠溶液和HCl混合液 | D. | 氯化钙 |
14.在密闭容器中,可逆反应N2+3H2?2NH3达到平衡后,若保持温度不变,缩小容器体积,达到新平衡时,下列说法正确的是( )
①NH3的浓度增大,N2和H2的浓度减小②NH3的物质的量增大,N2和H2的物质的量减小③H2的转化率增大,N2的转化率不变④混合气体的平均分子量增大.
①NH3的浓度增大,N2和H2的浓度减小②NH3的物质的量增大,N2和H2的物质的量减小③H2的转化率增大,N2的转化率不变④混合气体的平均分子量增大.
| A. | ①④ | B. | ②④ | C. | ①② | D. | ③④ |
11.已知1gH2完全燃烧生成水蒸气放出热量为121kJ,有关数据如下:O=O(键能为496kJ•mol-1)、H-H(键能为436kJ•mol-1),试求H2O(g)中H-O键的键能为( )
| A. | 463kJ•mol-1 | B. | 926kJ•mol-1 | C. | 1852kJ•mol-1 | D. | 920kJ•mol-1 |
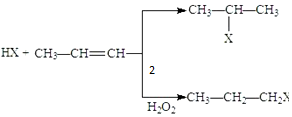 (X为卤素原子)
(X为卤素原子)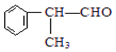 的物质,该物质是一种香料.
的物质,该物质是一种香料. $→_{催化剂}^{①CH_{2}=CH-CH_{3}}$A$→_{一氯代物}^{②光照}$B$\stackrel{③}{→}$C$→_{HCl}^{④}$D$\stackrel{⑤}{→}$E$\stackrel{⑥氧化反应}{→}$
$→_{催化剂}^{①CH_{2}=CH-CH_{3}}$A$→_{一氯代物}^{②光照}$B$\stackrel{③}{→}$C$→_{HCl}^{④}$D$\stackrel{⑤}{→}$E$\stackrel{⑥氧化反应}{→}$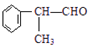
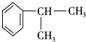 .
.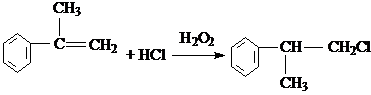 、2
、2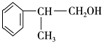 +O2$→_{△}^{Cu}$2
+O2$→_{△}^{Cu}$2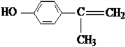 、
、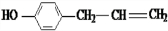 、
、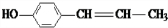 .
.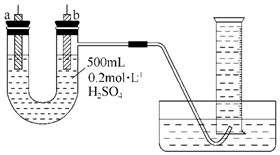 给你提供纯锌、纯铜片和500mL 0.2mol•L-1的H2SO4溶液、导线、1 000mL量筒.试用如图装置来测定锌和稀硫酸反应时在某段时间内通过导线的电子的物质的量.
给你提供纯锌、纯铜片和500mL 0.2mol•L-1的H2SO4溶液、导线、1 000mL量筒.试用如图装置来测定锌和稀硫酸反应时在某段时间内通过导线的电子的物质的量.