题目内容
11.已知1gH2完全燃烧生成水蒸气放出热量为121kJ,有关数据如下:O=O(键能为496kJ•mol-1)、H-H(键能为436kJ•mol-1),试求H2O(g)中H-O键的键能为( )| A. | 463kJ•mol-1 | B. | 926kJ•mol-1 | C. | 1852kJ•mol-1 | D. | 920kJ•mol-1 |
分析 化学反应放出的热量=新键生成释放的能量-旧键断裂吸收的能量.
解答 解:1gH2的物质的量n=$\frac{1g}{2g/mol}$=0.5mol,燃烧生成水蒸气放出热量为121KJ,可知2mol氢气完全燃烧生成水蒸气时放出热量484kJ,
则得出燃烧的热化学方程式:2H2(g)+O2(g)═2H2O(g)△H=-484kJ/mol,
设形成1mol H-O键完全断裂时吸收热量为X kJ,则:2H2(g)+O2(g)═2H2O(g)△H=-484kJ/mol,
436KJ×2 496KJ 4X
则有:436KJ×2+496KJ-4X=-484kJ
解得X=463KJ
故选A.
点评 本题考查反应热的有关计算,注意理解反应热与键能的关系,难度不大.

练习册系列答案
相关题目
2.科学家发现用二氧化钛(TiO2)作催化剂可以使水在光照条件下分解制得廉价的氢气,这使氢能源的研究和应用更向前迈进了一步.下列说法正确的是( )
| A. | 使用二氧化钛作催化剂使水快速分解的同时放出大量热 | |
| B. | 该过程涉及到的反应为氧化还原反应 | |
| C. | 该反应的原理是:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2+O2 | |
| D. | 每产生氢气44.8L,转移电子数目为2NA |
19.下列说法不正确的是( )
| A. | Mg(OH)2固体在溶液中存在平衡:Mg(OH)2(s)?Mg2+(aq)+2OH-(aq),该固体可溶于NH4Cl溶液 | |
| B. | 向ZnS沉淀上滴加CuSO4溶液沉淀变为黑色,可推知同温下Ksp(ZnS)<Ksp(CuS) | |
| C. | 向AgCl悬浊液中滴加Na2S溶液,白色沉淀变成黑色,反应方程式为2AgCl(s)+S2-(aq)?Ag2S(s)+2Cl-(aq) | |
| D. | 向2mL浓度均为1.2mol•L-1的KCl、KI混合溶液中滴加1~2滴0.01mol•L-1的AgNO3溶液,振荡沉淀呈黄色,说明Ksp(AgCl)>Ksp(AgI) |
6.以赤铁矿(主要成分为60.0%Fe2O3,杂质有3.6%FeO,Al2O3,MnO2,CuO等)为原料制备高活性铁单质的主要生产流程如图所示:
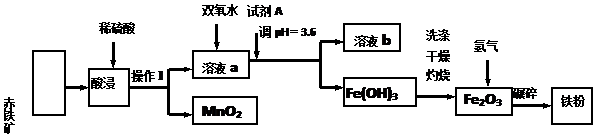
已知部分阳离子以氢氧化物形式完全深沉时溶液的pH如表所示,请回答下列问题:
(1)含杂质的赤铁矿使用前要将其粉碎,目的是增大固液接触面积,加快浸出反应速率,提高浸出率.操作Ⅰ的名称是过滤.
(2)将操作Ⅰ后所得的MnO2与KClO3、KOH溶液混合共热,可得到K2MnO4,此反应的化学方程式是3MnO2+KClO3+6KOH$\frac{\underline{\;\;△\;\;}}{\;}$3K2MnO4+KCl+3H2O.
(3)将PH控制在3.6的目的是使铁离子全部沉淀下来而其他金属离子不沉淀.已知25℃时,Ksp[Cu(OH)2]=2×10-20,该温度下反应Cu2++2H2O?Cu(OH)2+2H+的平衡常数K=5×10-9.
(4)加入双氧水时反应的离子方程式为H2O2+2Fe2++2H+=2Fe3++2H2O.
(5)利用氨气在500℃以上分解得到的氮原子渗透到铁粉中可制备氮化铁(FexVy),若消耗氨气17.0g,消耗赤铁矿石1Kg,写出该反应完整的化学方程式:16Fe+2NH3$\frac{\underline{\;大于500℃\;}}{\;}$2Fe8N+3H2.

已知部分阳离子以氢氧化物形式完全深沉时溶液的pH如表所示,请回答下列问题:
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Fe (OH)2 | Cu (OH)2 |
| pH | 3.4 | 5.2 | 9.7 | 6.7 |
(2)将操作Ⅰ后所得的MnO2与KClO3、KOH溶液混合共热,可得到K2MnO4,此反应的化学方程式是3MnO2+KClO3+6KOH$\frac{\underline{\;\;△\;\;}}{\;}$3K2MnO4+KCl+3H2O.
(3)将PH控制在3.6的目的是使铁离子全部沉淀下来而其他金属离子不沉淀.已知25℃时,Ksp[Cu(OH)2]=2×10-20,该温度下反应Cu2++2H2O?Cu(OH)2+2H+的平衡常数K=5×10-9.
(4)加入双氧水时反应的离子方程式为H2O2+2Fe2++2H+=2Fe3++2H2O.
(5)利用氨气在500℃以上分解得到的氮原子渗透到铁粉中可制备氮化铁(FexVy),若消耗氨气17.0g,消耗赤铁矿石1Kg,写出该反应完整的化学方程式:16Fe+2NH3$\frac{\underline{\;大于500℃\;}}{\;}$2Fe8N+3H2.
16.下列关于硫及其化合物的说法正确的是( )
| A. | 浓硫酸滴入胆矾中,胆矾失水变白,发生了化学变化 | |
| B. | 二氧化硫能使溴水褪色,体现二氧化硫的漂白性 | |
| C. | 浓硫酸与灼热的木炭反应,体现浓硫酸的强氧化性和酸性 | |
| D. | 加热时硫与铜反应生成黑色的硫化铜 |
3.下列溶液中粒子物质的量浓度的关系正确的是( )
| A. | pH相同的①NH4Cl②NH4Al(SO4)3③NH4HSO3,三种溶液中的c(NH4+):①<②<③ | |
| B. | 20mL0.1mol/L的CH3COONa溶液与10mL0.1mol/L的HCl溶液混合后呈酸性,所得溶液中:c(CH3COO-)>c(Cl-)>c(CH4COOH)>c(H+) | |
| C. | 0.1mol/L的NaHCO3溶液与0.1mol/L的NaOH溶液等体积混合,所得溶液中:c(Na+)>c(CO32-)>c(HCO3-)>c(OH-) | |
| D. | 常温下,pH=7的NH4Cl与氨水的混合溶液中:c(Cl-)>c(NH4+)>c(H+)=c(OH-) |
20.在一定条件下,Na2CO3溶液中存在CO32-+H2O?HCO3-+OH-平衡,下列说法正确的是( )
| A. | 稀释溶液,$\frac{c(HC{O}_{3}^{-}C)•c(O{H}^{-})}{c(C{O}_{3}^{2-})}$不变 | |
| B. | 通入CO2,溶液pH增大 | |
| C. | 升高温度,平衡常数减小 | |
| D. | 加入NaOH固体,$\frac{c(HC{O}_{3}^{-})}{c(C{O}_{3}^{2-})}$增大 |
1.下列物质制备的方程式正确的是( )
| A. | 实验室制氯气:MnO2+2Cl-+4H+$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O | |
| B. | 实验室制二氧化硫:Cu+SO42-+4H+$\frac{\underline{\;\;△\;\;}}{\;}$Cu2++SO2↑+2H2O | |
| C. | 实验室用浓氨水与生石灰制氨气:NH3•H2O+CaO═Ca(OH)2+NH3↑ | |
| D. | 实验室制二氧化氮:3Cu+4H++2NO3-═3Cu2++2NO2↑+2H2O |
 如图是制备Cu2O的电解池示意图,电解总反应为:2Cu+H2O$\stackrel{通电}{?}$Cu2O+H2↑.通电时,石墨电极发生还原反应(填“氧化”或“还原”);整个电解过程中,OH-的浓度不变(填“增大”或“减小”或“不变”).
如图是制备Cu2O的电解池示意图,电解总反应为:2Cu+H2O$\stackrel{通电}{?}$Cu2O+H2↑.通电时,石墨电极发生还原反应(填“氧化”或“还原”);整个电解过程中,OH-的浓度不变(填“增大”或“减小”或“不变”).