题目内容
14.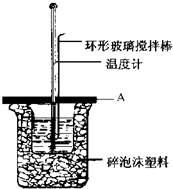 如图所示A为泡沫塑料板,上面有两个小孔,分别插入温度计和环形玻璃搅拌棒,两个小孔不能开得过大,其目的是减少热量损失; 若实验中不加盖泡沫塑料板,则求得的中和热数值(填偏大、偏小、无影响).
如图所示A为泡沫塑料板,上面有两个小孔,分别插入温度计和环形玻璃搅拌棒,两个小孔不能开得过大,其目的是减少热量损失; 若实验中不加盖泡沫塑料板,则求得的中和热数值(填偏大、偏小、无影响).
分析 根据测定中和热过程中必须尽量减少热量的散失分析;不盖硬纸板,会有一部分热量散失,据此判断测定误差.
解答 解:如图所示,A为泡沫塑料板,上面有两个小孔,分别插入温度计和环形玻璃搅拌棒,若两个小孔开得过大,会导致散失较多的热量,影响测定结果,所以两个小孔不能开得过大的目的是:减少热量损失;
大烧杯上若不盖硬纸板,会有一部分热量散失,求得的中和热数值将会减小,
故答案为:减少热量散失;偏小.
点评 本题考查了中和热的测定方法,题目难度不大,明确中和热的操作方法为解答关键,能够正确判断测定误差,试题培养了学生的分析能力及化学实验能力.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
9.在一密闭容器中,反应aA(g)+bB(g)?mC(s)+nD(g)达到平衡后,保持温度不变,将容器体积减小为原来体积的$\frac{1}{2}$,达到新的平衡时,D的浓度是原来的1.7倍,下列说法正确的是( )
| A. | 物质B的转化率增大 | B. | 平衡向正反应方向移动 | ||
| C. | 物质A的体积分数增大 | D. | a+b>m+n |
19.下列反应描述错误的是( )
| A. | Cu与过量浓HNO3反应,生成的气体呈红棕色 | |
| B. | 足量H2通过灼热的CuO粉末后,生成的固体为红色 | |
| C. | AgNO3溶液与足量Na2S溶液反应后再滴加NaCl溶液,沉淀为白色 | |
| D. | 物质的量相同的CH3COOH与NaOH反应后滴加酚酞,溶液显红色 |
4.下表中的实验操作能达到实验目的是( )
| 选项 | 实验操作 | 实验目的 |
| A | 将浓硫酸和碳单质混合加热,直接将生成的气体通入足量的澄清石灰水,石灰水变浑浊 | 检验气体产物中CO2的存在 |
| B | 将NaOH的乙醇溶液加入溴乙烷中,加热,将产生的气体直接通入到酸性高锰酸钾溶液中,溶液褪色 | 证明溴乙烷的消去反应有乙烯生成 |
| C | 先滴入Ba(NO3)2溶液,产生沉淀,加入足量稀盐酸,仍有沉淀 | 检验溶液中是否含有SO42- |
| D | 常温下测定物质的量浓度相同的盐酸和醋酸溶液的pH:盐酸pH小于醋酸pH | 证明相同条件下,在水中HCl电离程度大于CH3COOH |
| A. | A | B. | B | C. | C | D. | D |
 ⑤
⑤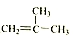
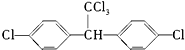
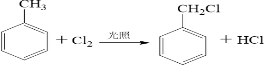
 _.
_.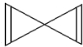 D.
D.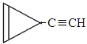 E.
E.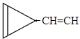



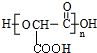 +(n-1)H2O.
+(n-1)H2O.
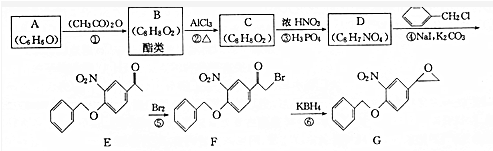
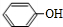 +(CH3CO)2O→
+(CH3CO)2O→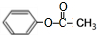 +CH3COOH.
+CH3COOH.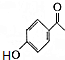 ;D的结构简式为
;D的结构简式为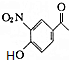 .
.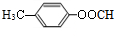 (填结构简式)
(填结构简式)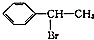 为起始原料制备
为起始原料制备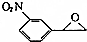 的合成路线:
的合成路线: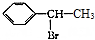 $→_{△}^{NaOH水溶液}$
$→_{△}^{NaOH水溶液}$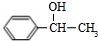 $→_{Cu/△}^{O_{2}}$
$→_{Cu/△}^{O_{2}}$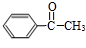 $→_{H_{3}PO_{4}}^{浓HNO_{3}}$
$→_{H_{3}PO_{4}}^{浓HNO_{3}}$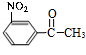 $\stackrel{NaBH_{4}}{→}$
$\stackrel{NaBH_{4}}{→}$