题目内容
20.金属钛(Ti)被誉为21世纪金属,具有良好的生物相容性,它兼具铁的高强度和铝的低密度.其单质和化合物具有广泛的应用价值.氮化钛(Ti3N4)为金黄色晶体,由于具有令人满意的仿金效果,越来越多地成为黄金的代替品.以TiCl4为原料,经过一系列反应可以制得Ti3N4和纳米TiO2(如图1).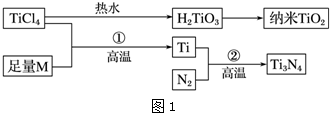
图1中的M是短周期金属元素,M的部分电离能如下表:
| I1 | I2 | I3 | I4 | I5 | |
| 电离能/kJ•mol-1 | 738 | 1451 | 7733 | 10540 | 13630 |
(1)Ti的基态原子外围电子排布式为4d25s2;
(2)M是Mg(填元素符号),该金属晶体的堆积模型为六方最密堆积,配位数为12;
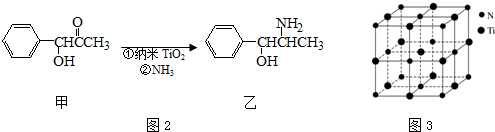
(3)纳米TiO2是一种应用广泛的催化剂,纳米TiO2催化的一个实例如图2所示.化合物甲的分子中采取sp2方式杂化的碳原子有7个,化合物乙中采取sp3方式杂化的原子对应的元素的电负性由大到小的顺序为O>N>C;
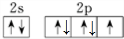
(4)有一种氮化钛晶体的晶胞与NaCl晶胞相似,如图3所示,该晶胞中N、Ti之间的最近距离为a pm,则该氮化钛的密度为$\frac{4×62}{{N}_{A}×(2a×1{0}^{-10})^{3}}$ g•cm-3(NA为阿伏加德罗常数的值,只列计算式).该晶体中与N原子距离相等且最近的N原子有12个;
(5)科学家通过X-射线探明KCl、MgO、CaO、TiN的晶体与NaCl的晶体结构相似.且知三种离子晶体的晶格能数据如下:
| 离子晶体 | NaCl | KCl | CaO |
| 晶格能/kJ•mol-1 | 786 | 715 | 3401 |
分析 (1)Ti原子核外电子数为22,根据能量最低原理书写;
(2)M是短周期金属元素,M的第三电离能剧增,处于ⅡA族,能与TiCl4反应置换出Ti,则M为Mg,Mg晶体属于六方最密堆积,配位数为12;
(3)采取sp2杂化的碳原子价层电子对数是3,采取sp3杂化的原子价层电子对数是4,乙中采取sp3杂化的原子有C、N、O,同一周期元素中,元素的电负性随着原子序数的增大;
(4)根据均摊法计算晶胞中Ti、N原子数目,进而计算晶胞质量,根据ρ=$\frac{m}{V}$计算晶胞密度;
以晶胞顶点N原子研究,与之距离相等且最近的N原子处于面心位置;
(5)由表中数据可知,离子半径越小晶格能越大,离子带电荷越大,晶格能越大,晶格能大,对应的离子晶体的熔点就越高.
解答 解:(1)Ti为22号元素,原子核外电子排布为1s22s22p63S23p63d24s2,外围电子排布式为4d25s2,
故答案为:4d25s2;
(2)M是短周期金属元素,M的第三电离能剧增,处于ⅡA族,能与TiCl4反应置换出Ti,则M为Mg.Mg晶体属于六方最密堆积,配位数为12,故答案为:Mg;12;
(3)化合物甲的分子中采取sp2杂化的碳原子为苯环上的六个、羰基中的一个,共7个;
采取sp3杂化的原子价层电子对数是4,乙中采取sp3杂化的原子有C、N、O,同一周期元素中,元素电负性随着原子序数依次增加电负性逐渐增大,所以它们的电负性关系为:O>N>C,
故答案为:7; O>N>C;
(4)根据均摊法,可知该晶胞中N原子个数为:6×$\frac{1}{2}$+8×$\frac{1}{8}$=4,该晶胞中Ti原子个数为:1+12×$\frac{1}{4}$=4,∴晶胞的质量m=4×$\frac{62}{{N}_{A}}$g,而晶胞的体积V=(2a×10-10)3cm3,所以晶体的密度ρ=4×$\frac{62}{{N}_{A}}$g÷(2a×10-10)3cm3=$\frac{4×62}{{N}_{A}(2a×1{0}^{-10})^{3}}$g•cm-3;
以晶胞顶点N原子研究,与之距离相等且最近的N原子处于面心位置,每个顶点为8个晶胞共用.每个面为2个晶胞共用,故与之距离相等且最近的N原子为$\frac{3×8}{2}$=12,
故答案为:$\frac{4×62}{{N}_{A}×(2a×1{0}^{-10})^{3}}$;12;
(5)离子晶体的离子半径越小,带电荷数越多,晶格能越大,则晶体的熔沸点越高,则有TiN>CaO,由表中数据可知CaO>KCl,则TiN>CaO>KCl,
故答案为:TiN>CaO>KCl.
点评 本题考查物质结构和性质,涉及等晶胞结构与计算、核外电子排布、杂化方式、电负性、晶体熔沸点比较等,注意理解电离能与最外层电子数关系,是对学生综合能力的考查,需要学生具备扎实的基础,难度中等.

| 元素编号 | 元素性质或原子结构 |
| R | 基态原子的最外层有3个未成对电子,次外层有2个电子 |
| S | 单质能与水剧烈反应,所得溶液呈弱酸性 |
| T | 基态原子3d轨道上有1个电子 |
| X |  |
(2)S元素的常见化合价为-1,其基态原子的价电子排布图为
(3)T元素的原子N能层上电子数为2.
(4)X的电子排布图违背了能量最低原理.用X单质、碱金属盐及碱土金属盐等可以做成焰火.燃放时,焰火发出五颜六色的光,请用原子结构的知识解释发光的原因:电子从能量较高的轨道跃迁到能量较低的轨道时,以光的形式释放能量.
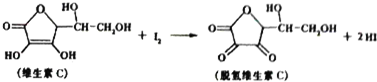
下列说法正确的是( )
| A. | 脱氢维生素C的分子式为C6H7O6 | B. | 上述反应为氧化反应 | ||
| C. | 滴定时反应剧烈振荡锥形瓶 | D. | 滴定时不可以用淀粉溶液作指示剂 |
| A. | 所含质子数=z | B. | 所含中子数=A-Z | C. | 所含电子数=Z+n | D. | 质量数=A |
| A. | 0.4 mol•L-1 | B. | 0.6 mol•L-1 | C. | 0.9 mol•L-1 | D. | 1.2 mol•L-1 |
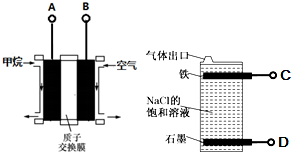
| A. | 燃料电池的A极连接电解池的C极 | |
| B. | A电极的电极反应式为:CH4-8e-+2H2O=CO2+8H+ | |
| C. | 燃料电池工作时H+移向左边 | |
| D. | 电解池总反应式为NaCl+H2O$\frac{\underline{\;电解\;}}{\;}$NaClO+H2↑ |
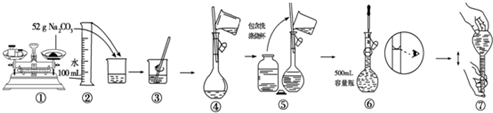
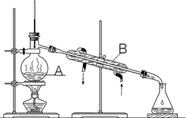 (1)指出图装置中A、B的名称
(1)指出图装置中A、B的名称