题目内容
11.现有部分前36号元素的性质或原子结构如下表:| 元素编号 | 元素性质或原子结构 |
| R | 基态原子的最外层有3个未成对电子,次外层有2个电子 |
| S | 单质能与水剧烈反应,所得溶液呈弱酸性 |
| T | 基态原子3d轨道上有1个电子 |
| X |  |
(2)S元素的常见化合价为-1,其基态原子的价电子排布图为
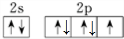
(3)T元素的原子N能层上电子数为2.
(4)X的电子排布图违背了能量最低原理.用X单质、碱金属盐及碱土金属盐等可以做成焰火.燃放时,焰火发出五颜六色的光,请用原子结构的知识解释发光的原因:电子从能量较高的轨道跃迁到能量较低的轨道时,以光的形式释放能量.
分析 (1)R基态原子的最外层有3个未成对电子,次外层有2个电子,其电子排布式为:1s22s22p3,则R为N元素;
(2)S单质能与水剧烈反应,所得溶液呈弱酸性,则S为F元素;
(3)T元素的基态原子3d轨道上有1个电子,核外电子排布式为1s22s22p63s23p63d14s2;
(4)X电子排布图违背能量最低原理,电子从能量较高的轨道跃迁到能量较低的轨道时,以光的形式释放能量,燃放时焰火发出五颜六色的光.
解答 解:(1)R基态原子的最外层有3个未成对电子,次外层有2个电子,其电子排布式为:1s22s22p3,则R为N元素,同周期相邻的元素为C、O,同周期随原子序数增大,元素第一电离能呈增大趋势,氮元素原子2p能级为半满稳定状态,能量较低,第一电离能高于同周期相邻元素的,故第一电离能:N>O>C,
故答案为:N>O>C;
(2)S单质能与水剧烈反应,所得溶液呈弱酸性,则S为F元素,非金属性最强,常见化合价为-1价,其基态原子的价电子排布图为: ,
,
故答案为:-1; ;
;
(3)T元素的基态原子3d轨道上有1个电子,核外电子排布式为1s22s22p63s23p63d14s2,原子N能层上电子数为2,
故答案为:2;
(4)基态原子应先填充满4s能级,再填充4p能级,X电子排布图违背能量最低原理,电子从能量较高的轨道跃迁到能量较低的轨道时,以光的形式释放能量,燃放时焰火发出五颜六色的光,
故答案为:能量最低原理;电子从能量较高的轨道跃迁到能量较低的轨道时,以光的形式释放能量.
点评 本题是对物质结构与性质的考查,注意理解同周期元素第一电离能异常情况,熟练掌握核外电子排布规律.

练习册系列答案
 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案
相关题目
19.下列物质属于有机物的是( )
| A. | 氰化钾(KCN) | B. | 碳酸(H2CO3) | C. | 甲烷(CH4 ) | D. | 碳化硅(SiC) |
6.下列电子书写正确的是( )
| A. | 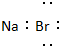 | B. |  | C. |  | D. |  |
16.茚是从煤油中提取的一种无色透明油状液体,不溶于水,可用于制造合成树脂.其结构简式为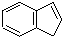 .下列关于茚的说法中不正确的是( )
.下列关于茚的说法中不正确的是( )
 .下列关于茚的说法中不正确的是( )
.下列关于茚的说法中不正确的是( )| A. | 茚能使酸性高锰酸钾溶液褪色 | |
| B. | 茚能使溴的四氯化碳溶液褪色 | |
| C. | 1 mol茚只含有1 mol碳碳双键 | |
| D. | 茚中所有的原子均可能处在同一平面上 |
3.为鉴别K2CO3和NaHCO3两种白色固体,有4位同学分别设计了以下四种不同的方案,其中方法和现象判断正确的是( )
| A. | 分别加入1mol/L的盐酸溶液,看有无气泡产生 | |
| B. | 分别取样配成溶液,滴加Ca(OH)2溶液,观察有无白色沉淀 | |
| C. | 用铂丝粘取固体在酒精灯火焰上灼烧,观察火焰的颜色,NaHCO3的焰色为紫色 | |
| D. | 分别取样在试管中加热,将可能产生的气体通入澄清石灰水,观察有无白色浑浊 |
20.金属钛(Ti)被誉为21世纪金属,具有良好的生物相容性,它兼具铁的高强度和铝的低密度.其单质和化合物具有广泛的应用价值.氮化钛(Ti3N4)为金黄色晶体,由于具有令人满意的仿金效果,越来越多地成为黄金的代替品.以TiCl4为原料,经过一系列反应可以制得Ti3N4和纳米TiO2(如图1).
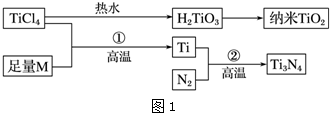
图1中的M是短周期金属元素,M的部分电离能如下表:
请回答下列问题:
(1)Ti的基态原子外围电子排布式为4d25s2;
(2)M是Mg(填元素符号),该金属晶体的堆积模型为六方最密堆积,配位数为12;
(3)纳米TiO2是一种应用广泛的催化剂,纳米TiO2催化的一个实例如图2所示.化合物甲的分子中采取sp2方式杂化的碳原子有7个,化合物乙中采取sp3方式杂化的原子对应的元素的电负性由大到小的顺序为O>N>C;
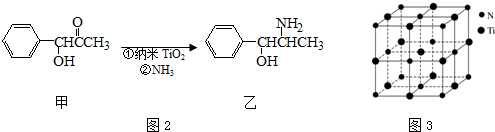
(4)有一种氮化钛晶体的晶胞与NaCl晶胞相似,如图3所示,该晶胞中N、Ti之间的最近距离为a pm,则该氮化钛的密度为$\frac{4×62}{{N}_{A}×(2a×1{0}^{-10})^{3}}$ g•cm-3(NA为阿伏加德罗常数的值,只列计算式).该晶体中与N原子距离相等且最近的N原子有12个;
(5)科学家通过X-射线探明KCl、MgO、CaO、TiN的晶体与NaCl的晶体结构相似.且知三种离子晶体的晶格能数据如下:
KCl、CaO、TiN三种离子晶体熔点由高到低的顺序为TiN>CaO>KCl.

图1中的M是短周期金属元素,M的部分电离能如下表:
| I1 | I2 | I3 | I4 | I5 | |
| 电离能/kJ•mol-1 | 738 | 1451 | 7733 | 10540 | 13630 |
(1)Ti的基态原子外围电子排布式为4d25s2;
(2)M是Mg(填元素符号),该金属晶体的堆积模型为六方最密堆积,配位数为12;
(3)纳米TiO2是一种应用广泛的催化剂,纳米TiO2催化的一个实例如图2所示.化合物甲的分子中采取sp2方式杂化的碳原子有7个,化合物乙中采取sp3方式杂化的原子对应的元素的电负性由大到小的顺序为O>N>C;

(4)有一种氮化钛晶体的晶胞与NaCl晶胞相似,如图3所示,该晶胞中N、Ti之间的最近距离为a pm,则该氮化钛的密度为$\frac{4×62}{{N}_{A}×(2a×1{0}^{-10})^{3}}$ g•cm-3(NA为阿伏加德罗常数的值,只列计算式).该晶体中与N原子距离相等且最近的N原子有12个;
(5)科学家通过X-射线探明KCl、MgO、CaO、TiN的晶体与NaCl的晶体结构相似.且知三种离子晶体的晶格能数据如下:
| 离子晶体 | NaCl | KCl | CaO |
| 晶格能/kJ•mol-1 | 786 | 715 | 3401 |
1.有A、B两种烃,其相关信息如下
回答下列问题:
(1)烃A的最简式是CH;
(2)烃A的结构简式是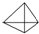 ;
;
(3)烃B的3种二溴代物的结构简式为CHBr2CH(CH3)2;CH2BrCBr(CH3)2;CH2BrCH(CH3)CH2Br.
| A | 完全燃烧的产物中n(CO2):n(H2O)=2:1 28<Mr(A)<60 不能使溴的四氯化碳溶液褪色 一氯代物只有1种结构 |
| B | 饱和链烃,通常情况下呈气态 二溴代物有3种 |
(1)烃A的最简式是CH;
(2)烃A的结构简式是
 ;
;(3)烃B的3种二溴代物的结构简式为CHBr2CH(CH3)2;CH2BrCBr(CH3)2;CH2BrCH(CH3)CH2Br.
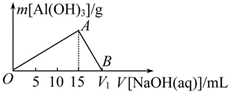 向20mL某浓度的AlCl3溶液中滴加2mol•L-1的NaOH溶液时,所得沉淀的质量与加入NaOH溶液的体积之间的关系如图所示:
向20mL某浓度的AlCl3溶液中滴加2mol•L-1的NaOH溶液时,所得沉淀的质量与加入NaOH溶液的体积之间的关系如图所示: