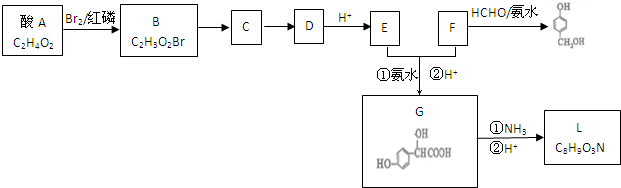
题目内容
移取25.00mL HAc试液,以酚酞为指示剂,用0.1002mol/L NaOH标准滴定溶液滴定至终点,消耗21.26mL,求试液中醋酸的含量(以g/L表示)[M(HAc)=60.05g/mol].
考点:化学方程式的有关计算
专题:计算题
分析:发生HAc+NaOH=NaCl+H2O,滴定至终点时,n(HAc)=n(NaOH),以此计算.
解答:
解:发生HAc+NaOH=NaCl+H2O,滴定至终点时,n(HAc)=n(NaOH)=0.1002mol/L×21.26mL×0.001L/mL=2.13×10-3mol,
则试液中醋酸的含量为
=5.12g/L,
答:试液中醋酸的含量为5.12g/L.
则试液中醋酸的含量为
| 2.13×10-3mol×60.05g/mol |
| 25×10-3L |
答:试液中醋酸的含量为5.12g/L.
点评:本题考查化学反应的计算,为高频考点,把握发生的反应及物质的量关系为解答的关键,侧重酸碱中和反应计算的考查,题目难度不大.

练习册系列答案
相关题目
在一定条件下将A和B加入密闭容器中发生反应:A(g)+B(s)?2C(g).忽略固体体积,平衡时C的体积分数随温度和压强的变化如下表所示(“-”为未测数据).
下列说法正确的是( )
| 1.0 | 2.0 | 3.0 | |
| 810 | 54.0 | - | a |
| 915 | - | 75.0 | - |
| 1000 | - | b | 83.0 |
| A、△S<0 |
| B、915℃2.0MPa,A的转化率为60% |
| C、a>b |
| D、平衡常数:K(1000℃)<K(810℃) |
以Pt作电极,用电源串联电解分装在两个烧杯里的200mL 0.3mol/L NaCl溶液和300mL 0.2mol/L的CuSO4溶液,过一段时间取出电极,将两杯溶液混合,则对混合溶液的pH判断正确的是( )
| A、小于7 | B、大于7 |
| C、小于或等于7 | D、大于7或等于7 |
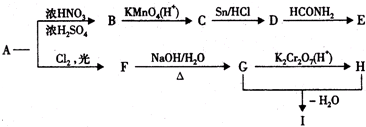
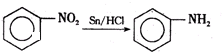
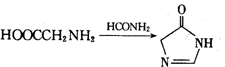
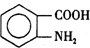 ,物质E含2个六元环.
,物质E含2个六元环.