题目内容
9.取1.43g Na2CO3•10H2O溶于水配成100ml溶液,求:(1)Na2CO3物质的量浓度;
(2)取出20ml该溶液用蒸馏水稀释,使Na2CO3溶液物质的量浓度变为0.004mol/L,所用容量瓶的规格是多大?
分析 (1)根据n=$\frac{m}{M}$计算1.43gNa2CO3•10H2O的物质的量,n(Na2CO3)=n(Na2CO3•10H2O),根据c=$\frac{n}{V}$计算所得溶液中Na2CO3的物质的量浓度;
(2)稀释碳酸钠的浓度为0.04mol/L,根据稀释定律计算稀释后溶液的体积,进而计算加入蒸馏水的体积.
解答 解:(1)1.43gNa2CO3•10H2O的物质的量=$\frac{1.43g}{286g/mol}$=0.005mol,n(Na2CO3)=n(Na2CO3•10H2O)=0.005mol,配成100mL溶液,Na2CO3物质的量浓度为$\frac{0.005mol}{0.1L}$=0.05mol/L,
答:Na2CO3物质的量浓度为0.05mol/L;
(2)取出20ml该溶液用蒸馏水稀释,使Na2CO3溶液物质的量浓度变为0.004mol/L,令稀释后溶液的体积为VmL,根据稀释定律,
0.05mol/L×20mL=0.04mol/L×V mL,
解得V=25,
故加入蒸馏水的体积为25mL-20mL=5mL,
答:需要加入水的体积为5mL.
点评 本题考查物质的量浓度有关计算,比较基础,注意对物质的量浓度定义式的理解与灵活应用,侧重于考查学生的分析能力和计算能力.

练习册系列答案
相关题目
8.下列叙述中正确的是( )
| A. | 氯原子、氯离子、氯气均为黄绿色,且氯离子比氯原子结构稳定 | |
| B. | 氯原子易得电子,所以Cl2在化学反应中氯元素化合价只会降低 | |
| C. | 氯原子、氯离子、氯气分子中原子的最外层均达到8电子结构 | |
| D. | 氯元素在自然界中不存在游离态,只以化合态形式存在 |
17. 煤化工是以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业过程.
煤化工是以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业过程.
(1)将水蒸气通过红热的碳即可产生水煤气.反应为:
C(s)+H2O(g)?CO(g)+H2(g)
一定温度下,在一个容积固定的密闭容器中,发生上述反应,下列能判断该反应达到化学平衡状态的是bc.(填字母)
a.容器中的压强不再改变
b.1mol H-H键断裂的同时断裂2mol H-O键
c.v正(CO)=v逆(H2O)
d.c(CO)=c(H2)
(2)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应CO(g)+H2O(g)?CO2(g)+H2(g),得到如下三组数据:
实验1中以v(CO)表示的反应速率为0.16mol/(L•min).
(3)目前工业上有一种方法是用CO2来生产甲醇.一定条件下发生反应:
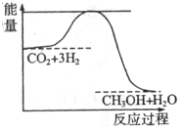
CO2(g)+3H2(g)?CH3OH(g)+H2O(g),如图表示该反应进行过程中能量的变化.在体积为1L的恒容密闭容器中,充入1mol CO2和3mol H2反应达到平衡后,降低温度能使c(CH3OH)增大(填“增大”“减小”或“不变”).
 煤化工是以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业过程.
煤化工是以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业过程.(1)将水蒸气通过红热的碳即可产生水煤气.反应为:
C(s)+H2O(g)?CO(g)+H2(g)
一定温度下,在一个容积固定的密闭容器中,发生上述反应,下列能判断该反应达到化学平衡状态的是bc.(填字母)
a.容器中的压强不再改变
b.1mol H-H键断裂的同时断裂2mol H-O键
c.v正(CO)=v逆(H2O)
d.c(CO)=c(H2)
(2)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应CO(g)+H2O(g)?CO2(g)+H2(g),得到如下三组数据:
| 实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
| H2O | CO | H2 | CO | |||
| 1 | 650 | 2 | 4 | 1.6 | 2.4 | 5 |
| 2 | 900 | 1 | 2 | 0.4 | 1.6 | 3 |
(3)目前工业上有一种方法是用CO2来生产甲醇.一定条件下发生反应:
CO2(g)+3H2(g)?CH3OH(g)+H2O(g),如图表示该反应进行过程中能量的变化.在体积为1L的恒容密闭容器中,充入1mol CO2和3mol H2反应达到平衡后,降低温度能使c(CH3OH)增大(填“增大”“减小”或“不变”).
14.下列既属于无机物,又属于碱的是( )
| A. | Na2CO3 | B. | CH4 | C. | CH3CH2OH | D. | Cu(OH)2 |
1.用石墨做电极电解下列溶液,通电一段时间后溶液的pH变大的是( )
| A. | NaCl溶液 | B. | NaOH溶液 | C. | H2SO4溶液 | D. | CuSO4溶液 |
19.下列微粒半径大小顺序正确的是( )
| A. | O2->F->Na+>Mg2+ | B. | Na>Mg>Cl>Ar | C. | I>Br>F>Cl | D. | Na>Na+>S2->S |
 A、B、C为短周期元素,在周期表中所处的位置如图所示.
A、B、C为短周期元素,在周期表中所处的位置如图所示.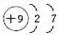 ,C的单质与水反应的化学方程式为2F2+2H2O=4HF+O2;
,C的单质与水反应的化学方程式为2F2+2H2O=4HF+O2;