题目内容
19.下列微粒半径大小顺序正确的是( )| A. | O2->F->Na+>Mg2+ | B. | Na>Mg>Cl>Ar | C. | I>Br>F>Cl | D. | Na>Na+>S2->S |
分析 粒子的电子层越多,粒子半径越大,电子层相同时,粒子的核电荷数越大,离子半径越小;当核电荷数、核外电子层数都相等时,核外电子总数越多,微粒半径越大,注意同一周期中稀有气体的原子半径较大,据此进行解答.
解答 解:A.四种离子的电子层相同,核电荷数越大,离子半径越小,则离子半径大小为:O2->F->Na+>Mg2+,故A正确;
B.同一周期中,稀有气体的原子半径较大,则Ar的原子半径大于Na,故B错误;
C.同一主族元素,核电荷数越大,原子半径越小,则原子半径:I>Br>Cl>F,故C错误;
D.Na+的电子层最少,其离子半径最小,Na、S2-、S的核外电子层数都是3,核电荷数越大,微粒半径越小;当核电荷数、电子层相同时,核外电子总数越多,微粒半径越大,则微粒半径大小为:Na>S2->S>Na+,故D错误;
故选A.
点评 本题考查了元素周期律内容的综合应用,题目难度不大,试题侧重考查微粒半径大小比较,明确粒子比较大小规律为解答关键,试题培养了学生的灵活应用能力.

练习册系列答案
 教材全解字词句篇系列答案
教材全解字词句篇系列答案
相关题目
10.我国钨资源矿产丰富.由黑钨矿提取钨发生的反应之一为:3H2+WO3$\frac{\underline{\;高温\;}}{\;}$W+3H2O.其基本反应类型是( )
| A. | 化合反应 | B. | 分解反应 | C. | 置换反应 | D. | 复分解反应 |
7.下列反应既属于氧化还原反应,又是吸热反应的是( )
| A. | 锌粒与稀硫酸的反应 | |
| B. | 灼热的木炭与CO2反应 | |
| C. | 甲烷在氧气中的燃烧反应 | |
| D. | Ba(OH)2•8H2O晶体与NH4Cl晶体的反应 |
14.下列说法正确的是( )
| A. | 铜基态原子核外电子排布式为1s22s22p63s23p64s13d10 | |
| B. | 在d轨道中电子排布成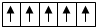 而不是 而不是 ,其最直接的根据是泡利原理 ,其最直接的根据是泡利原理 | |
| C. | 下列轨道的能量是按由高到低排列的E5s>E4s>E3d>E2p>E1s | |
| D. | 焰色反应、激光、霓虹灯光等与原子核外电子发生跃迁释放能量有关 |
4.下列电子式中错误的是( )
| A. | Na+ | B. | 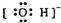 | C. | 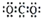 | D. | 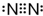 |
11.下列气体中,既能用碱石灰干燥,又能用排水法收集的是( )
| A. | CO | B. | NO2 | C. | SO2 | D. | NH3 |