题目内容
在120g的CuO固体中,通过标准状况下NH344.8L,在加热条件下反应生成Cu、N2和H2O,反应后得固体100g.求:
(1)氨的利用率;(2)反应中电子转移的物质的量.
(1)氨的利用率;(2)反应中电子转移的物质的量.
考点:化学方程式的有关计算
专题:计算题
分析:根据反应方程式2NH3+3CuO
3Cu+N2+3H2O,结合固体质量变化,来分析求解.
| ||
解答:
解:设参加反应的氨的物质的量为xmol,则
2NH3+3CuO
3Cu+N2+3H2O,固体质量变化
2mol 48
xmol 120-100
即
=
,解之得:x=0.83mol,所以利用率为:
×100%=41.5%;
反应中3mol的氧化铜反应转移6mol电子,所以转移电子的物质的量为:0.83mol×2=1.66mol,
答:(1)氨的利用率为:41.5%;(2)反应中电子转移的物质的量为:1.66mol.
2NH3+3CuO
| ||
2mol 48
xmol 120-100
即
| 2mol |
| xmol |
| 48 |
| 20 |
| 0.83mol | ||
|
反应中3mol的氧化铜反应转移6mol电子,所以转移电子的物质的量为:0.83mol×2=1.66mol,
答:(1)氨的利用率为:41.5%;(2)反应中电子转移的物质的量为:1.66mol.
点评:本题考查由反应方程式求物质的得用率和转移电子的物质的量,学生只要用差量法求解即可,比较容易.

练习册系列答案
相关题目
向1L 0.5mol/L的NaOH溶液中加入下列物质:①稀醋酸 ②浓硫酸 ③稀硝酸,恰好完全反应放出的热量分别为Q1、Q2、Q3,三者的关系正确的是( )
| A、Q1>Q2>Q3 |
| B、Q1<Q3<Q2 |
| C、Q1<Q2<Q3 |
| D、Q1>Q3>Q2 |
某高分子化合物的结构如图,它的单体是( )


A、 |
B、 |
| C、苯和乙烷 |
| D、苯和乙烯 |
下列说法正确的是( )
| A、葡萄糖和淀粉均属于高分子化合物 |
| B、鸡蛋清中加入 CuSO4 溶液会产生盐析 |
| C、14C可用于文物年代的鉴定,14C与14N互为同位素 |
| D、自由移动离子数目多的电解质溶液导电能力不一定强 |
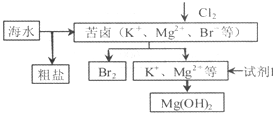 海洋约占地球表面积的71%,对其进行开发利用的部分流程如图所示.下列说法不正确的是( )
海洋约占地球表面积的71%,对其进行开发利用的部分流程如图所示.下列说法不正确的是( )| A、可用BaCl2溶液除去粗盐中的SO42- |
| B、从苦卤中提取Br2的离子方程式为2Br-+Cl2═2C1-十Br2 |
| C、试剂1可以选用Ca(OH)2 |
| D、工业上,电解熔融Mg(OH)2冶炼金属镁 |
化学与生产、生活密切相关,下列说法不正确的是( )
| A、Al2O3熔点高,可用于制作耐高温仪器 |
| B、明矾净水与胶体的性质有关 |
| C、H7N9型禽流感病毒在高温条件下被杀死的过程是蛋白质变性 |
| D、高纯度的硅单质用于制作光导纤维,光导纤维有导电性 |
今有如下三个热化学方程式:
H2(g)+
O2(g)═H2O(g)△H=a kJ?mol-1
H2(g)+
O2(g)═H2O(l)△H=b kJ?mol-1
2H2(g)+O2(g)═2H2O(l)△H=c kJ?mol-1
关于它们的下列表述,正确的是( )
H2(g)+
| 1 |
| 2 |
H2(g)+
| 1 |
| 2 |
2H2(g)+O2(g)═2H2O(l)△H=c kJ?mol-1
关于它们的下列表述,正确的是( )
| A、它们都是吸热反应 |
| B、氢气的燃烧热为△H=a kJ?mol-1 |
| C、反应热的关系:a=b |
| D、反应热的关系:2b=c |

