题目内容
15.某原电池总反应为Cu+2FeCl3=2FeCl2+CuCl2,完成下列填空题正极反应:2Fe3++2e-=2Fe2+负极反应:Cu-2e-=Cu2+ 电解质溶液FeCl3溶液.
分析 由方程式可知,Cu被氧化,为原电池的负极,则正极可为碳棒,电解质溶液为氯化铁溶液,正极发生还原反应,负极发生氧化反应,以此解答该题.
解答 解:由方程式Cu+2FeCl3=CuCl2+2FeCl2可知,Cu被氧化,为原电池的负极,负极反应为Cu-2e-=Cu2+,正极Fe3+被还原,电极方程式为2Fe3++2e-=2Fe2+,则电解质溶液为FeCl3溶液;
故答案为:2Fe3++2e-=2Fe2+;Cu-2e-=Cu2+;FeCl3溶液.
点评 本题考查了原电池的原理,注意把握负极材料和电解质溶液的成分,一般来说,还原剂作负极,不如负极活泼的金属或非金属导体作正极,氧化剂的溶液作电解质溶液,题目难度不大.

练习册系列答案
 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案
相关题目
5.碳酸镍可用于电镀、陶瓷器着色等.镍矿渣中镍元素的主要存在形式是Ni(OH)2和NiS(含有Fe、Cu、Ca、Mg、Zn等元素杂质),从镍矿渣出发制备碳酸镍的流程如下:
已知:常温下,部分物质的溶度积常数如表:
(1)浸取过程中欲加快浸取速率,可采用的措施之一是将矿石粉碎(或提高浸取时的温度,或适当增大酸的浓度等合理答案均可);
(2)浸取出Ni2+时反应的离子方程式有①Ni(OH)2+2H+=Ni2++2H2O②NiS+ClO3-+H+→Ni2++S+Cl-+H2O(未配平),此反应中还原产物与氧化产物的物质的量比为1:3.
(3)加入Na2CO3溶液沉铁时生成难溶于水的黄钠铁矾[NaFe3(SO4)2(OH)6]和一种无色气体.写出此反应的离子方程式:3Fe3++3CO32-+Na++2SO42-+3H2O=NaFe3(SO4)2(OH)6+3CO2↑.
(4)加入NiS的作用是除去溶液中的Cu2+,反应的离子方程式为:Cu2++NiS=Ni2++CuS,过滤后,溶液中c(Ni2+)=0.107 mol•L-1时,溶液中残留c(Cu2+)为1.27×10-16mol•L-1.
(5)加入NaF的作用是除去Ca2+,有机萃取剂用于除去Zn2+.

已知:常温下,部分物质的溶度积常数如表:
难溶物 | NiS | ZnS | CuS | CaF2 | MgF2 |
| 溶度积常数 | 1.07×10-21 | 2.93×10-25 | 1.27×10-36 | 1.46×10-10 | 7.42×10-11 |
(2)浸取出Ni2+时反应的离子方程式有①Ni(OH)2+2H+=Ni2++2H2O②NiS+ClO3-+H+→Ni2++S+Cl-+H2O(未配平),此反应中还原产物与氧化产物的物质的量比为1:3.
(3)加入Na2CO3溶液沉铁时生成难溶于水的黄钠铁矾[NaFe3(SO4)2(OH)6]和一种无色气体.写出此反应的离子方程式:3Fe3++3CO32-+Na++2SO42-+3H2O=NaFe3(SO4)2(OH)6+3CO2↑.
(4)加入NiS的作用是除去溶液中的Cu2+,反应的离子方程式为:Cu2++NiS=Ni2++CuS,过滤后,溶液中c(Ni2+)=0.107 mol•L-1时,溶液中残留c(Cu2+)为1.27×10-16mol•L-1.
(5)加入NaF的作用是除去Ca2+,有机萃取剂用于除去Zn2+.
6.下列说法不正确的是( )
| A. | 除去蛋白质中的葡萄糖,可以用浓硫酸铵溶液盐析过滤方法提纯 | |
| B. | 双氧水中滴加氯化铁溶液立即产生气泡,说明氯化铁的氧化性比过氧化氢强 | |
| C. | 锂钒氧化物蓄电池放电时电池的总反应式为:V2O5+xLi═LixV2O5.供电时Li+向正极移动,充电时阳极的电极反应式为:LixV2O5-xe-═V2O5+xLi+ | |
| D. | 常温下,Mg(OH)2能溶于氯化铵浓溶液的主要原因是NH4+结合OH-使沉淀溶解平衡发生移动 |
10.解释下列物质性质的变化规律时,与共价键的键能无关的是( )
| A. | N2比O2的化学性质稳定 | B. | F2、Cl2、Br2、I2的沸点逐渐升高 | ||
| C. | 金刚石的熔点比晶体硅高 | D. | HF、HCl、HBr、HI的热稳定性依减弱 |
20.在化学试卷的开始处有“可能用到的相对原子质量”一项,如H:1 C:12 Cl:35.5 S:32等.请问对这些数值准确的说法应该是( )
| A. | 某种核素的相对原子质量的近似值 | B. | 某种核素的相对原子质量 | ||
| C. | 某种元素的相对原子质量的近似值 | D. | 某种元素的相对原子质量 |
7.有下列离子晶体立体结构示意图:
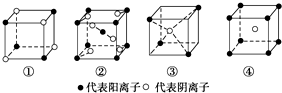
若以M代表阳离子,以R代表阴离子,则各离子晶体的组成表达式完全正确的组合是( )

若以M代表阳离子,以R代表阴离子,则各离子晶体的组成表达式完全正确的组合是( )
| A. | ①MR ②MR2 ③MR3 ④MR4 | B. | ①MR ②MR2 ③MR2 ④MR | ||
| C. | ①MR2 ②MR2 ③MR2 ④MR | D. | ①MR ②MR ③MR2 ④MR2 |
4.右图是部分短周期主族元素原子半径与原子序数的关系图.下列说法错误的是( )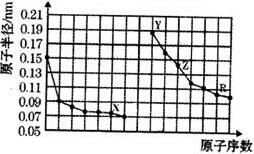

| A. | X、Y两种单质在常温下反应生成的产物为碱性氧化物 | |
| B. | Z2R3可由Y2R和ZCl3的溶液反应制取 | |
| C. | Y、Z、R三种元素对应的最高价氧化物的水化物相互之间可以发生反应 | |
| D. | 电解熔融的X与Z构成的化合物可以得到单质Z |



 .
. .
. .
.