题目内容
18.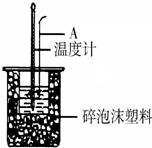 利用如图装置测定中和热的实验步骤如下
利用如图装置测定中和热的实验步骤如下①量取50mL 0.25mol/L H2SO4溶液倒入小烧杯中,测量温度;
②量取50mL 0.55mol/L NaOH溶液,测量温度;
③将NaOH溶液倒入小烧杯中,混合均匀后测量混合液温度.请回答:
(1)如图所示,仪器A的名称是环形玻璃搅拌棒.
(2)NaOH溶液稍过量的原因确保硫酸被完全中和.
(3)加入NaOH溶液的正确操作是B(填字母).
A.沿玻璃棒缓慢加入 B.一次迅速加入 C.分三次加入
(4)上述实验测得的结果与书上的57.3kJ/mol有偏差,产生偏差的原因可能是abc
a.实验装置保温、隔热效果差
b.NaOH溶液倒入盛有硫酸的小烧杯中后未及时将盖板盖好.
c.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
(5)不能(填“能”或“不能”)用Ba(OH)2代替氢氧化钠溶液和稀硫酸反应,理由是H2SO4与Ba(OH)2反应除生成水外,还会发生Ba2+,SO42-的反应,该反应也会有热效应.
(6)若将含0.5mol H2SO4的浓硫酸与含1mol NaOH的溶液混合,放出的热量大于(填“小于”、“等于”或“大于”)57.3kJ,原因是浓硫酸溶于水放出热量.
(7)已知:CH3COOH(aq)与NaOH(aq)反应的△H=-12.1kJ•mol-1;HCl(aq)与NaOH(aq)反应的△H=-55.6kJ•mol-1.则CH3COOH在水溶液中电离的△H等于C.
A.-67.7kJ•mol-1 B.-43.5kJ•mol-1 C.+43.5kJ•mol-1 D.+67.7kJ•mol-1.
分析 (1)仪器A的名称环形玻璃搅拌棒;
(2)为了确保定量的硫酸反应完全,所用NaOH稍过量;
(3)将NaOH溶液倒入小烧杯中,不能分几次倒入,否则会导致热量散失,影响测定结果;
(4)a.装置保温、隔热效果差,测得的热量偏小;
b.NaOH溶液倒入盛有硫酸的小烧杯中后未及时将盖板盖好,热量散失较多;
c.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度,H2SO4的起始温度偏高;
(5)氢氧化钡与硫酸反应生成了硫酸钡沉淀,生成沉淀的过程中会有热量变化,影响测定结果;
(6)浓硫酸稀释放热,放出热量;
(7)CH3COOH(aq)与NaOH(aq)反应可分为两步:①CH3COOH在水溶液中电离CH3COOH?H++CH3COO-;②产生的H+与NaOH(aq)反应,利用盖斯定律进行计算,可得CH3COOH在水溶液中电离的反应热.
解答 解:(1)如图所示,仪器A的名称是环形玻璃搅拌棒;
故答案为:环形玻璃搅拌棒;
(2)实验中,所用NaOH稍过量的原因是确保定量的硫酸反应完全,
故答案为:确保硫酸被完全中和;
(3)倒入氢氧化钠溶液时,必须一次迅速的倒入,目的是减少热量的散失,不能分几次倒入氢氧化钠溶液,否则会导致热量散失,影响测定结果,
故答案为:B;
(4)a.装置保温、隔热效果差,测得的热量偏小,中和热的数值偏小,故a正确;
b.NaOH溶液倒入盛有硫酸的小烧杯中后未及时将盖板盖好,热量散失较多,测得温度偏低,中和热的数值偏小,故b正确;
c.温度计测定NaOH溶液起始温度后直接插入盐酸测温度,盐酸的起始温度偏高,温度差偏小,测得的热量偏小,中和热的数值偏小,故c正确;
故答案为:abc;
(5)硫酸与Ba(OH)2溶液反应除了生成水外,还生成了BaSO4沉淀,该反应也会有热效应,所以不能用Ba(OH)2溶液和硫酸代替NaOH溶液和盐酸测中和热.
故答案为:不能;H2SO4与Ba(OH)2反应除生成水外,还会发生Ba2+,SO42-的反应,该反应也会有热效应;
(6)由于浓硫酸稀释放热,若将含0.5molH2SO4的浓硫酸与含1molNaOH的溶液混合,放出的热量大于57.3kJ;
故答案为:大于;浓硫酸溶于水放出热量;
(7)CH3COOH(aq)+OH-(aq)═CH3COO-(aq)+H2O(l)△H=-12.1kJ•mol-1 ①
H+(aq)+OH-(aq)═H2O(l)△H=△H=-55.6kJ•mol-1 ②
用①-②可得CH3COOH电离的热化学方程式为:CH3COOH(aq)?H+(aq)+CH3COO-(aq)△H=-12.1kJ•mol-1-(-55.6kJ•mol-1)=+43.5kJ•mol-1;
故选C.
点评 本题主要考查中和热的测定、盖斯定律的运用,题目难度大,注意理解中和热的概念、反应热的误差分析等问题.

 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案①实验室制乙炔时用饱和食盐水与电石反应,并用硫酸铜溶液除杂质
②重结晶法提纯苯甲酸时,为了析出更多晶体,热滤液用冰盐水充分冷却
③只用水一种试剂可以鉴别乙醇、甲苯、硝基苯
④用己烯萃取碘酒中的碘
⑤检验溴乙烷中的溴元素:向NaOH水溶液中先加几滴溴乙烷,加热,充分反应后,冷却,再加入AgNO3溶液,观察现象.
| A. | ①③⑤ | B. | ②④⑤ | C. | ②③④ | D. | ①③④ |
| A. | C2H4 | B. | CH4 | C. | CH3COOCH2CH3 | D. | C2H5OH |
| A. | 溴苯 | B. | 苯 | C. | 环己烷 | D. | 硝基苯 |
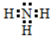 ;实验室制备气体A的化学方程式2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2H2O+2NH3↑.
;实验室制备气体A的化学方程式2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2H2O+2NH3↑.