题目内容
7.将下列物质注入水中,振荡后静置,能分层且沉于水面下的是( )| A. | 溴苯 | B. | 苯 | C. | 环己烷 | D. | 硝基苯 |
分析 注入水中,振荡后静置,能分层且沉于水面下,说明有机物不溶于水,且密度比水大,以此解答该题.
解答 解:题中涉及物质都不溶于水,溶液分层,其中苯、己烷的密度比水小,在水上面,溴苯、硝基苯密度比水大,在水面以下,
故选AD.
点评 本题考查混合物分离、提纯方法,为高频考点,把握物质的性质为解答的关键,侧重分液及物质密度的考查,注意常见有机物的溶解性,题目难度不大.

练习册系列答案
相关题目
3. 一定温度下在密闭容器内进行着某一反应,X气体、Y气体的物质的量随反应时间变化的曲线如图.下列叙述中正确的是( )
一定温度下在密闭容器内进行着某一反应,X气体、Y气体的物质的量随反应时间变化的曲线如图.下列叙述中正确的是( )
 一定温度下在密闭容器内进行着某一反应,X气体、Y气体的物质的量随反应时间变化的曲线如图.下列叙述中正确的是( )
一定温度下在密闭容器内进行着某一反应,X气体、Y气体的物质的量随反应时间变化的曲线如图.下列叙述中正确的是( )| A. | 反应的化学方程式为5Y?X | B. | t1时,Y的浓度是X浓度的2倍 | ||
| C. | t2时,正、逆反应速率相等 | D. | t3时,正、逆反应速率相等 |
12.某同学到了傍晚时就看不见东西,患了夜盲症,他体内缺少的维生素可能是( )
| A. | 维生素D | B. | 维生素C | C. | 维生素B | D. | 维生素A |
17. BHT是一种常用的食品抗氧化剂,从
BHT是一种常用的食品抗氧化剂,从 出发合成BHT的方法有如下两种.下列说法错误的是( )
出发合成BHT的方法有如下两种.下列说法错误的是( )
 BHT是一种常用的食品抗氧化剂,从
BHT是一种常用的食品抗氧化剂,从 出发合成BHT的方法有如下两种.下列说法错误的是( )
出发合成BHT的方法有如下两种.下列说法错误的是( )| A. | 从绿色化学角度分析方法一优于方法二 | |
| B. | BHT在水中的溶解度小于苯酚 | |
| C. | 两种方法的反应类型都是加成反应 | |
| D. | BHT与 都能使酸性KMnO4溶液褪色 都能使酸性KMnO4溶液褪色 |
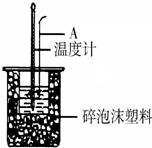 利用如图装置测定中和热的实验步骤如下
利用如图装置测定中和热的实验步骤如下



