��Ŀ����
6������ʵ�������ʵ�鷽����Ʋ���ȷ���У���������ʵ��������Ȳʱ�ñ���ʳ��ˮ���ʯ��Ӧ����������ͭ��Һ������
���ؽᾧ���ᴿ������ʱ��Ϊ���������ྦྷ�壬����Һ�ñ���ˮ�����ȴ
��ֻ��ˮһ���Լ����Լ����Ҵ����ױ���������
���ü�ϩ��ȡ����еĵ�
�ݼ����������е���Ԫ�أ���NaOHˮ��Һ���ȼӼ��������飬���ȣ���ַ�Ӧ����ȴ���ټ���AgNO3��Һ���۲�����
| A�� | �٢ۢ� | B�� | �ڢܢ� | C�� | �ڢۢ� | D�� | �٢ۢ� |
���� �����������ͭ��Һ��Ӧ���������Ե���ͭ��
�ڿ���ȴ�����£�����Ҫ�ñ���ˮ�����ȴ��
���Ҵ�����ˮ���ױ�����������ˮ�����ܣ��ױ��ܶ�С��ˮ���������ܶȴ���ˮ��
���ѻ������к��в����������ܺ͵ⷴӦ��
�����������£������Ӻ������ӷ������ӷ�Ӧ��
��� �⣺����ȡ����Ȳ�����к����������壬���������ͭ��Һ��Ӧ���������Ե���ͭ���Ӷ���ȥ���ʣ��ʢ���ȷ��
�ڱ�������ܽ�����¶ȱ仯�ϴ�Ϊ���������ྦྷ�壬��ȴ�����¼��ɣ��ʢڴ���
���Ҵ�����ˮ���ױ�����������ˮ�����ܣ��ױ��ܶ�С��ˮ���������ܶȴ���ˮ�����Էֱ��ˮ���ʱ����ͬ���ʢ���ȷ��
���ѻ������к��в����������ܺ͵ⷢ���ӳɷ�Ӧ�����Բ������ѻ�������ȡ�⣬�ʢܴ���
�����������£������Ӻ������ӷ������ӷ�Ӧ���������������ӵļ�����Ҫ�����кͼ�ʢݴ���
��ѡB��
���� ���⿼����ʵ�鷽�����ۣ���Ŀ�Ѷ��еȣ���ȷʵ��ԭ���ǽⱾ��ؼ����������ʵ���������������״�ѡ���Ǣݣ��ܶ�ͬѧ����©���кͼ�����´���Ϊ�״��㣮

��ϰ��ϵ�д�
 ͨ��ѧ��Ĭд����ϵ�д�
ͨ��ѧ��Ĭд����ϵ�д�
�����Ŀ
2��������ʵ���Ũ�ȵ�NaOH��Na2CO3�Ļ����Һ�м���ϡ���ᣮ�������ӷ���ʽ����ʵ��������ǣ�������
| A�� | OH-+CO32-+2H+�THCO3-+H2O | B�� | 2OH-+CO32-+3H+�THCO3-+2H2O | ||
| C�� | OH-+CO32-+3H+�TCO2��+2H2O | D�� | 2OH-+CO32-+4H+�TCO2��+3H2O |
3�� һ���¶������ܱ������ڽ�����ijһ��Ӧ��X���塢Y��������ʵ����淴Ӧʱ��仯��������ͼ��������������ȷ���ǣ�������
һ���¶������ܱ������ڽ�����ijһ��Ӧ��X���塢Y��������ʵ����淴Ӧʱ��仯��������ͼ��������������ȷ���ǣ�������
 һ���¶������ܱ������ڽ�����ijһ��Ӧ��X���塢Y��������ʵ����淴Ӧʱ��仯��������ͼ��������������ȷ���ǣ�������
һ���¶������ܱ������ڽ�����ijһ��Ӧ��X���塢Y��������ʵ����淴Ӧʱ��仯��������ͼ��������������ȷ���ǣ�������| A�� | ��Ӧ�Ļ�ѧ����ʽΪ5Y?X | B�� | t1ʱ��Y��Ũ����XŨ�ȵ�2�� | ||
| C�� | t2ʱ�������淴Ӧ������� | D�� | t3ʱ�������淴Ӧ������� |
20����NA��ʾ�����ӵ������ģ�����˵����ȷ���ǣ�������
| A�� | 32 g������O2����32g������O3��������ԭ������Ϊ2NA | |
| B�� | 18gˮ������������Ϊ8NA | |
| C�� | ���³�ѹ�£�1 mol����ԭ����Ϊ2NA | |
| D�� | ���³�ѹ�£�111.2L����������ԭ����ΪNA |
1�����������У���һ����������ˮ��ĸ߷��ӻ������ǣ�������
| A�� | ���� | B�� | ��֬ | C�� | ��ά�� | D�� | ������ |

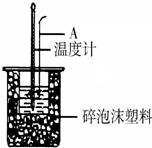 ������ͼװ�òⶨ�к��ȵ�ʵ�鲽������
������ͼװ�òⶨ�к��ȵ�ʵ�鲽������