题目内容
强弱电解质的本质区别是( )
| A、导电能力 | B、化学键的类型 |
| C、溶解度 | D、电离程度 |
考点:强电解质和弱电解质的概念
专题:电离平衡与溶液的pH专题
分析:强电解质是指:在水溶液中或熔融状态下,能够完全电离的化合物.即溶于水的部分或者熔融状态时,可以完全变成阴阳离子的化合物.一般是强酸、强碱和大部分盐类.弱电解质是指:在水溶液里部分电离的电解质,包括弱酸、弱碱、水与少数盐.据此即可解答.
解答:
解:A.电解质的强弱与电离程度有关,与溶液的导电能力无关,溶液的导电性强弱取决于溶液中离子浓度的大小,离子浓度越大,导电性越强,如硫酸钡是强电解质,但它难溶于水,虽溶于水的部分能完全电离,可导电能力很弱,故A错误;
B.化学键分为离子键和共价键、金属键,共价键为非金属原子之间形成的化学键,离子键为阴阳离子之间形成的化学键,金属键为金属离子和电子之间形成的化学键,离子化合物含有活泼的金属和活泼非金属,一般为强电解质,共价化合物既有强电解质,也有弱电解质,如氯化氢是共价化合物,它是强电解质,乙酸也是共价化合物,但它是弱酸,是弱电解质,所以强弱电解质的本质区别与化学键的类型无关,故B错误;
C.强弱电解质与溶解度无关,如硫酸钡是强电解质,但它难溶于水,乙酸易溶于水,但它是弱酸,是弱电解质,故C错误;
D.强电解质是指:在水溶液中或熔融状态下,能够完全电离的化合物.即溶于水的部分或者熔融状态时,可以完全变成阴阳离子的化合物,故D正确;
故选D.
B.化学键分为离子键和共价键、金属键,共价键为非金属原子之间形成的化学键,离子键为阴阳离子之间形成的化学键,金属键为金属离子和电子之间形成的化学键,离子化合物含有活泼的金属和活泼非金属,一般为强电解质,共价化合物既有强电解质,也有弱电解质,如氯化氢是共价化合物,它是强电解质,乙酸也是共价化合物,但它是弱酸,是弱电解质,所以强弱电解质的本质区别与化学键的类型无关,故B错误;
C.强弱电解质与溶解度无关,如硫酸钡是强电解质,但它难溶于水,乙酸易溶于水,但它是弱酸,是弱电解质,故C错误;
D.强电解质是指:在水溶液中或熔融状态下,能够完全电离的化合物.即溶于水的部分或者熔融状态时,可以完全变成阴阳离子的化合物,故D正确;
故选D.
点评:本题考查了强弱电解质与导电能力、溶解度之间的关系,难度不大,抓住强电解质的定义中的关键词“完全电离”是解题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列叙述正确的是( )
| A、变质的油脂有难闻的特殊气味,是由于油脂发生了水解反应 |
| B、高温或日常用的消毒剂可使禽流感病毒蛋白质变性 |
| C、棉花、羊毛、木材和草类的主要成分都是纤维素 |
| D、误食重金属盐引起人体中毒,可喝大量的食盐水解毒 |
已知某温度下,Ksp(AgCl)=1.56×10-10 mol2?L-2,Ksp(Ag2CrO4)=1.12×10-12 mol3?L-3,下列叙述正确的是( )
| A、向氯化银的浊液中加入氯化钠溶液,氯化银的Ksp减小 |
| B、向2.0×10-4mol?L-1的K2CrO4溶液中加入等体积的2.0×10-4 mol?L-1 AgNO3溶液,则有Ag2CrO4沉淀生成 |
| C、将一定量的AgCl和Ag2CrO4固体混合物溶于蒸馏水中,充分溶解后,静置,上层清液中Cl-的物质的量浓度最大 |
| D、将0.001 mol?L-1的AgNO3溶液逐滴滴入0.001 mol?L-1的KCl和0.001 mol?L-1的K2CrO4的混合溶液中,则先产生AgCl沉淀 |
化学与生产、生活和社会可持续发展密切相关.下列说法不正确的是( )
| A、二氧化硅可用于制造光导纤维 |
| B、小苏打可用于面粉发酵 |
| C、酒精可用作汽车燃料 |
| D、明矾可用于自来水杀菌消毒 |
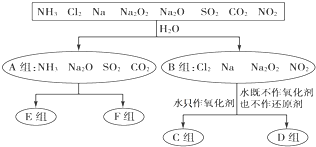
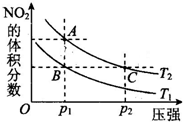 请回答下列问题
请回答下列问题