题目内容
25.6g铜与一定量的浓硝酸反应,生成8.96L的NO和NO2.将生成的气体和一定量的O2通入水中,问最少需要多少L的O2?
考点:氧化还原反应的计算
专题:守恒法
分析:反应中Cu失去电子,N得到电子;将生成的气体和一定量的O2通入水中,气体恰好吸收时,N失去电子、O得到电子,则结合电子守恒计算.
解答:
解:反应中Cu失去电子,N得到电子;将生成的气体和一定量的O2通入水中,气体恰好吸收时,N失去电子、O得到电子,
Cu的物质的量为
=0.4mol,
由电子守恒可知,需要氧气为
=0.2mol,
其体积为0.2mol×22.4L/mol=4.48L,
答:需要4.48L的O2.
Cu的物质的量为
| 25.6g |
| 64g/mol |
由电子守恒可知,需要氧气为
| 0.4mol×2 |
| 2×(2-0) |
其体积为0.2mol×22.4L/mol=4.48L,
答:需要4.48L的O2.
点评:本题考查氧化还原反应的计算,为高频考点,把握反应中元素的化合价变化及电子守恒为解答的关键,侧重分析与计算能力的考查,题目难度不大.

练习册系列答案
相关题目
强弱电解质的本质区别是( )
| A、导电能力 | B、化学键的类型 |
| C、溶解度 | D、电离程度 |
将容积为50mL的量筒充满二氧化氮和氧气的混合气体,将量筒倒置在盛满水的水槽里,一段时间后,量筒里剩余气体体积为5mL.则原混合气体中NO2和O2体积比可能是( )
| A、9:1 | B、18:7 |
| C、41:9 | D、1:1 |
有关AgCl的沉淀溶解平衡的说法正确的是( )
| A、AgCl难溶于水,溶液中没有Ag+和Cl- |
| B、AgCl沉淀生成和溶解同时在不断进行,且速率相等 |
| C、向AgCl溶液中加入盐酸,一定会有沉淀生成 |
| D、向含有AgCl的悬浊液中加入NaBr固体,AgCl沉淀不变化 |
下列条件下,两物质所含分子数不相等的是( )
| A、同温度、相同质量的N2和CO |
| B、常温常压,同体积的H2O和O2 |
| C、同压强、同物质的量的N2和O2 |
| D、同体积、同密度的N2和CO |
下列关于各图象的解释或结论正确的是( )
A、.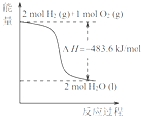 热化学方程式是H2(g)+
| ||
B、.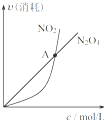 对于恒温恒容条件下的反应2NO2(g)?N2O4(g),A点为平衡状态 | ||
C、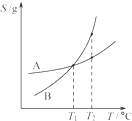 将A、B饱和溶液分别由T1℃升温至T2℃时,溶质的质量分数B>A | ||
D、.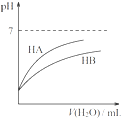 同温度、同浓度的NaA溶液与NaB溶液相比,其pH前者小于后者 |
NA表示阿伏加德罗常数,下列说法中正确的是( )
| A、在常温下,22.4L氧气所含的分子总数为NA |
| B、在标准状况下,NA个CO2分子与NA个H2SO4分子所占的体积之比为1:1 |
| C、标准准况下,22.4L 乙醇中含有NA个乙醇分子 |
| D、在1L 0.1mol/L的碳酸钠溶液中,所含Na+的数目为0.2NA |
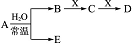 已知由 C、N、O、Na、Fe五种元素组成的常见单质或化合物存在如图所示转化关系(部分生成物和反应条件略去).
已知由 C、N、O、Na、Fe五种元素组成的常见单质或化合物存在如图所示转化关系(部分生成物和反应条件略去).