题目内容
A、B、C、D 4种元素的核电荷数依次增大,它们的离子的电子层数相同且最外层电子数均为8.A原子的L层电子数与K、M层电子数之和相等,D原子的K、L层电子数之和等于电子总数的一半.请回答下列问题:
(1)4种元素的符号依次是A ,B ,C ,D .它们原子半径由大到小的顺序是 .
(2)它们离子的半径由大到小的顺序是 .
(3)已知AB能形成一种分子式为AB2的化合物,写出其电子式 .
(1)4种元素的符号依次是A
(2)它们离子的半径由大到小的顺序是
(3)已知AB能形成一种分子式为AB2的化合物,写出其电子式
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:A、B、C、D 4种元素的核电荷数依次增大,A原子的L层电子数与K、M层电子数之和相等,则M层电子数=8-2=6,故A为S元素;D原子的K、L层电子数之和等于电子总数的一半,则L层已经排满电子,故核外电子数=2×(2+8)=20,故D为Ca元素,四元素的离子的电子层数相同且最外层电子数均为8,结合原子序数,可推知,B为Cl、C为K,据此解答.
解答:
解:A、B、C、D 4种元素的核电荷数依次增大,A原子的L层电子数与K、M层电子数之和相等,则M层电子数=8-2=6,故A为S元素;D原子的K、L层电子数之和等于电子总数的一半,则L层已经排满电子,故核外电子数=2×(2+8)=20,故D为Ca元素,四元素的离子的电子层数相同且最外层电子数均为8,结合原子序数,可推知,B为Cl、C为K,
(1)由上述分析可知,A为S,B为Cl,C为K,D为Ca,电子层数越多,原子半径越大,电子层娄相同,核电荷数越大,原子半径越小,所以原子半径r(K)>r(Ca)>r(S)>r(Cl),
故答案为:S;Cl;K;Ca;r(K)>r(Ca)>r(S)>r(Cl);
(2)电子层结构相同,核电荷数越大,离子半径越小,故离子半径r(S2-)>r(Cl-)>r(K+)>r(Ca2+),
故答案为:r(S2-)>r(Cl-)>r(K+)>r(Ca2+);
(3)已知AB能形成一种分子式为AB2的化合物为SCl2,它的电子式为 ,故答案为:
,故答案为: .
.
(1)由上述分析可知,A为S,B为Cl,C为K,D为Ca,电子层数越多,原子半径越大,电子层娄相同,核电荷数越大,原子半径越小,所以原子半径r(K)>r(Ca)>r(S)>r(Cl),
故答案为:S;Cl;K;Ca;r(K)>r(Ca)>r(S)>r(Cl);
(2)电子层结构相同,核电荷数越大,离子半径越小,故离子半径r(S2-)>r(Cl-)>r(K+)>r(Ca2+),
故答案为:r(S2-)>r(Cl-)>r(K+)>r(Ca2+);
(3)已知AB能形成一种分子式为AB2的化合物为SCl2,它的电子式为
 ,故答案为:
,故答案为: .
.
点评:本题主要考查了半径比较、电子式等知识,难度不大,元素推断是解题的关键,答题时注意第(3)问,根据8电子稳定结构写电子式.

练习册系列答案
 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案
相关题目
将2.0molPCl3和2.0molCl2充入体积不变的1L密闭容器中,在一定条件下发生下述反应:PCl3(g)+Cl2(g)?PCl5(g) 达到平衡时,PCl5为1.0mol;如果此时将PCl3和Cl2全部移走,在相同温度下再达平衡时PCl5的物质的量是( )
| A、0.38mol |
| B、0.50mol |
| C、0.62mol |
| D、无法确定 |
有关化学原理的说法或比较正确的是( )
| A、对于可逆反应来说,反应物只有按等物质的量投料,其转化率才能相等 |
| B、AgCl悬浊液中存在平衡:AgCl(s)?Ag+ (aq)+Cl-(aq),往其中加入少量NaCl粉末,平衡向左移动,溶液中离子的总浓度会减小 |
| C、常温下0.1 mol/L的下列溶液 ①NH4Al(SO4)2、②NH4Cl、③NH3?H2O、④CH3COONH4中c (NH4+)由大到小的顺序是:②>①>④>③ |
| D、等浓度的下列稀溶液:①硫酸氢钠、②乙酸钠、③醋酸、④碳酸氢钠、⑤硝酸钠、⑥苯酚钠,它们的PH由小到大排列的为:①③⑤②④⑥ |
下列图示与对应叙述相符合的是( )
A、 如图:反应N2+3H2?2NH3在恒温情况下,反应速率与压强的关系 |
B、 如图:反应H2+I2?2HI 达平衡后,升高温度时反应速率随时间的变化 |
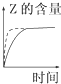
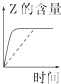
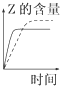
C、 如图:反应CO2(g)+H2(g)?CO(g)+H2O(g)△H>0,水蒸气含量随时间的变化 |
D、 如图:反应2SO2+O2?2SO3 达平衡后,缩小容器体积时各成分的物质的量随时间的变化 |
下列可逆反应达到平衡后,增大压强同时降低温度,平衡一定向右移动的是( )
| A、2AB(g)?A2(g)+B2(g)△H>0 |
| B、A2(g)+3B2(g)?2AB3(g)△H<0 |
| C、A(s)+B(g)?C(g)+D(g)△H>0 |
| D、2A(g)+B(g)?3C(g)+D(s)△H<0 |
下列化学式与指定物质的主要成分对应正确的是( )
| A、CH4--天然气 |
| B、CO2--水煤气 |
| C、CuSO4?5H2O--明矾 |
| D、NaHCO3--苏打粉 |