题目内容
下列可逆反应达到平衡后,增大压强同时降低温度,平衡一定向右移动的是( )
| A、2AB(g)?A2(g)+B2(g)△H>0 |
| B、A2(g)+3B2(g)?2AB3(g)△H<0 |
| C、A(s)+B(g)?C(g)+D(g)△H>0 |
| D、2A(g)+B(g)?3C(g)+D(s)△H<0 |
考点:化学平衡的影响因素
专题:化学平衡专题
分析:根据增大压强同时降低温度,平衡一定向右移动,则说明增大压强平衡向右移动或者不移动,降低温度平衡也向右移动,据此分析.
解答:
解:增大压强同时降低温度,平衡一定向右移动,则说明增大压强平衡向右移动或者不移动,降低温度平衡也向右移动,所以该反应应该是气体体积减小或者不变的放热反应,
故选:BD.
故选:BD.
点评:本题考查化学平衡的影响因素,题目难度不大,解答时首先分析化学方程式的特征,特别是反应前后气体的化学计量数关系以及反应的吸、放热问题.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
用水稀释0.1mol/L氨水时,溶液中随水量的增加而减小的是( )
A、
| ||
B、
| ||
| C、c(H+) | ||
| D、n(OH-) |
温度相同,向甲、乙两体积相同的密闭容器中,各通入2mol SO2和1mol O2发生反应;2SO2(g)+O2(g)?2SO3(g)达到平衡时,甲容器中SO2的转化率大于乙容器中SO2的转化率.下列判断正确的是( )
| A、甲保持压强不变,乙保持体积不变 |
| B、甲保持体积不变,乙保持压强不变 |
| C、混合气体密度甲小于乙 |
| D、混合气体的平均相对分子质量甲小于乙 |
下列说法正确的是( )
| A、被氧化的物质是氧化剂 |
| B、可以利用酒精将碘水中的碘提取出来 |
| C、化合反应一定不是氧化还原反应 |
| D、铝抗腐蚀是外层氧化膜致密的缘故 |
四种短周期元素在元素周期表中的相对位置如图所示,w的气态氢化物可与其最高价含氧酸反应生成离子化合物,由此可知( )
| W | X | |
| Y | Z |
| A、X元素形成的单核阴离子还原性强于Y的 |
| B、Z元素氧化物对应水化物的酸性一定强于Y |
| C、X、Y、Z中最简单氮化物稳定性最差的是Y |
| D、z元素单质在化学反应中只表现氧化性 |
研究反应物的化学计量数与产物之间的关系时,使用类似数轴的方法可以收到的直观形象的效果.下列表达不正确的是( )
A、密闭容器中CuO和C高温反应的气体产物: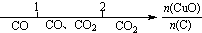 |
B、Fe在Cl2中的燃烧产物: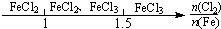 |
C、NaOH溶液中通入一定量的CO2的产物: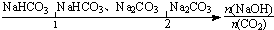 |
D、AlCl3溶液中滴加NaOH溶液后体系中铝元素的存在形式: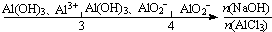 |
下列有关说法正确的是( )
| A、反应NH3(g)+HCl(g)═NH4Cl(s)在室温下可自发进行,则该反应的△H<0 |
| B、0.01 mol/L的氨水可以使酚酞试液变红,说明氨水是弱电解质 |
| C、FeCl3溶液和Fe2(SO4)3溶液加热蒸干、灼烧都得到Fe2O3 |
| D、在化学平衡、电离平衡、水解平衡中,平衡常数都随温度的升高而增大 |