题目内容
5.实验室制氯气的尾气处理用NaOH(或KOH)溶液吸收,其化学反应方程式为Cl2+2NaOH═NaCl+NaClO+H2O (或Cl2+2KOH═KCl+KClO+H2O)..分析 氯气有毒,不能排放在环境中,利用NaOH溶液或KOH溶液吸收,以此来解答.
解答 解:实验室制氯气的尾气处理用NaOH(或KOH)溶液吸收,其化学反应方程式为Cl2+2NaOH═NaCl+NaClO+H2O (或Cl2+2KOH═KCl+KClO+H2O),
故答案为:NaOH(或KOH);Cl2+2NaOH═NaCl+NaClO+H2O (或Cl2+2KOH═KCl+KClO+H2O).
点评 本题考查氯气的制备实验中尾气的处理,为高频考点,把握氯气的性质、化学与环境的关系为解答的关键,侧重分析与应用能力的考查,注意尾气吸收要彻底,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
15.下列有关甲烷的叙述正确的是( )
| A. | 天然气的主要成分甲烷燃烧时放出大量热量,属于重要的二次能源 | |
| B. | 甲烷分子中四个碳氢单键的性质完全相同,分子结构为平面正方形 | |
| C. | 甲烷和氯气反应生成的二氯甲烷没有同分异构现象 | |
| D. | 甲烷的化学性质比较稳定,不被任何氧化剂氧化 |
16.下列反应过程中,先有沉淀生成,后沉淀又会消失的是( )
| A. | 将氨水逐滴滴入Al2(SO4)3溶液中,直至过量 | |
| B. | 在AlCl3溶液中逐滴滴入NaOH溶液,直至过量 | |
| C. | 在NaOH 溶液中逐滴滴入 MgSO4 溶液,直至过量 | |
| D. | 在 Na2SiO3溶液中逐滴滴入盐酸,直至过量 |
20.下列叙述中正确的是( )
| A. | 同一主族元素原子序数越大的单质的熔点、沸点也越高 | |
| B. | 除H外,周期表中主族族序数等于周期数的元素全为金属元素 | |
| C. | 同主族的非金属的简单氢化物中最稳定的其熔、沸点也最高 | |
| D. | 同周期的主族元素形成的简单离子的半径从左到右依次减小 |
17.如表为元素周期表的一部分.
请参照①~⑧的位置,用化学用语回答问题:
(1)①的元素名称是锂,其在周期表中的位置是第2周期ⅠA族.
(2)②③④的原子半径由大到小的顺序是C>N>O(用元素符号表示).
(3)⑦⑧的最高价含氧酸的酸性由强到弱的顺序是H3PO4>H2SiO3(用化学式表示).
(4)⑥的最高价氧化物与⑤的最高价氧化物对应的水化物反应的离子方程式是Al2O3+2OH-=2AlO2-+H2O.
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | ||||||||
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
(1)①的元素名称是锂,其在周期表中的位置是第2周期ⅠA族.
(2)②③④的原子半径由大到小的顺序是C>N>O(用元素符号表示).
(3)⑦⑧的最高价含氧酸的酸性由强到弱的顺序是H3PO4>H2SiO3(用化学式表示).
(4)⑥的最高价氧化物与⑤的最高价氧化物对应的水化物反应的离子方程式是Al2O3+2OH-=2AlO2-+H2O.
14.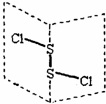 二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,其分子结构如图所示.常温下,S2Cl2遇水易与水发生反应,并产生能使品红褪色的气体,下列说法中错误的是( )
二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,其分子结构如图所示.常温下,S2Cl2遇水易与水发生反应,并产生能使品红褪色的气体,下列说法中错误的是( )
 二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,其分子结构如图所示.常温下,S2Cl2遇水易与水发生反应,并产生能使品红褪色的气体,下列说法中错误的是( )
二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,其分子结构如图所示.常温下,S2Cl2遇水易与水发生反应,并产生能使品红褪色的气体,下列说法中错误的是( )| A. | S2Cl2的结构式为 Cl-S-S-Cl | |
| B. | S2Cl2与水反应时只有S-Cl断裂 | |
| C. | S2Br2含有极性键和非极性键 | |
| D. | S2Cl2与H2O反应的化学方程式可能为:2S2Cl2+2H2O=SO2↑+3S↓+4HCl |

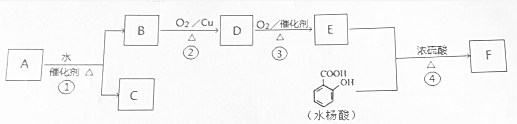
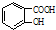 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$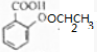 +H2O.
+H2O.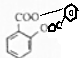 +H2O.
+H2O.