题目内容
2.将20mL充满NO和NO2的混合气体的试管倒立于盛水的水槽中,充分反应后,剩余气体的体积为10mL,原混合气体中NO体积(气体体积处于同温同压下)( )| A. | 5 ml | B. | 10 ml | ||
| C. | 15 ml | D. | 条件不足,无法计算 |
分析 二氧化氮和水反应的方程式为:3NO2+H2O═2HNO3+NO,一氧化氮和水不反应,利用差量法计算参加反应的二氧化氮体积,再根据质量守恒计算一氧化氮的体积.
解答 解:设二氧化氮为xmL,因为NO与水不反应,所以不会引起气体体积变化,二氧化氮与水反应3NO2+H2O═2HNO3+NO,依据方程式可知:
3NO2+H2O═2HNO3+NO△V
3 3-1
x (20-10)mL
则:$\frac{3}{x}=\frac{3-1}{(20-10)mL}$,解得:x=15mL,
则原混合气体中NO体积为:V(NO)=20mL-15mL=5mL,
故选A.
点评 本题考化学方程式的计算,题目难度不大,明确二氧化氮和水的反应、利用差量法来计算是解本题的关键,试题培养了学生的分析能力及化学计算能力.

练习册系列答案
相关题目
11.化学知识在生活中有重要意义,下列说法不正确的是( )
| A. | 在食品袋中放入盛有硅胶和铁粉的透气小袋,可防止食物受潮、氧化变质 | |
| B. | 小苏打用于治疗胃溃疡病人的胃酸过多症 | |
| C. | 液氨汽化时要吸收大量的热,常用作制冷剂 | |
| D. | 纯净的二氧化硅是生产光纤制品的基本原料 |
13.设NA为阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 标准状况下,0.56 L丙烷中含有共价键的数目为0.2NA | |
| B. | 常温常压下,6.4 g氧气和臭氧中含有的原子总数为0.4NA | |
| C. | 5.6 g铁与一定量硝酸恰好反应,转移的电子数目一定为0.3NA | |
| D. | 常温下,2 L 0.1 mol•L-1Na2CO3溶液中,含有的CO32-离子数为0.2NA |
10.1mol Na2O2晶体和1mol Na2O的晶体中阴离子的个数比较,前者和后者的关系是( )
| A. | 前者大 | B. | 前者小 | C. | 相等 | D. | 不能肯定 |
17.写出以下有机物的官能团名称并判断物质类别:
(1)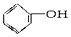 (2)CH2=CH-CH3 (3)CH3COOCH3(4)CH3-CHO (5)CH3-OH (6)CH3CH2COOH.
(2)CH2=CH-CH3 (3)CH3COOCH3(4)CH3-CHO (5)CH3-OH (6)CH3CH2COOH.
(1)
 (2)CH2=CH-CH3 (3)CH3COOCH3(4)CH3-CHO (5)CH3-OH (6)CH3CH2COOH.
(2)CH2=CH-CH3 (3)CH3COOCH3(4)CH3-CHO (5)CH3-OH (6)CH3CH2COOH.| 物质序号 | 物质类别 | 官能团名称 | 物质序号 | 物质类别 | 官能团名称 |
| (1) | (4) | ||||
| (2) | (5) | ||||
| (3) | (6) |
7.下列属于吸热反应的是( )
| A. | 铝粉与氧化铁的反应 | B. | 氯化铵与氢氧化钡的反应 | ||
| C. | 锌片与稀硫酸反应 | D. | 钠与冷水反应 |
14.设NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 42 g C3H6中含有的共用电子对数目为8 NA | |
| B. | 电解饱和食盐水时,当0.1 mol NaCl反应时,转移的电子数为0.1 NA | |
| C. | 常温常压下,22.4 L N2和O2的混合气体中含有的分子数目为NA | |
| D. | 1 L 0.01 mol•L-1 KAl(SO4)2溶液中含有的阳离子数目为0.02 NA |
11.化学与科学、技术、社会、环境密切相关,下列过程没有发生化学变化的是( )
| A. | 用热碱液清除炊具上残留的油污 | |
| B. | 用浸泡过高锰酸钾溶液的硅藻土保鲜水果 | |
| C. | 用含硅胶、铁粉的透气小袋和食品一起密封包装 | |
| D. | 用活性炭去除冰箱中的异味 |
12.化学与人类生产、生活、社会可持续发展密切相关,下列说法正确的是( )
| A. | 明矾净水的原理和家用消毒液消毒的原理相同,都能起到消毒杀菌作用 | |
| B. | 聚乙烯、聚氯乙烯都是高分子化合物,但聚氯乙烯薄膜不能用于包装食品 | |
| C. | “天宫一号”使用的碳纤维,是一种新型有机高分子材料 | |
| D. | 铝合金的大量使用,归功于人们能用焦炭等还原剂从氧化铝中获得铝 |