题目内容
12.化学与人类生产、生活、社会可持续发展密切相关,下列说法正确的是( )| A. | 明矾净水的原理和家用消毒液消毒的原理相同,都能起到消毒杀菌作用 | |
| B. | 聚乙烯、聚氯乙烯都是高分子化合物,但聚氯乙烯薄膜不能用于包装食品 | |
| C. | “天宫一号”使用的碳纤维,是一种新型有机高分子材料 | |
| D. | 铝合金的大量使用,归功于人们能用焦炭等还原剂从氧化铝中获得铝 |
分析 A.明矾水溶液中铝离子水解生成具有吸附性氢氧化铝胶体,具有吸附性;
B.聚氯乙烯受热分解产生有毒物质;
C.碳纤维,主要成分为碳单质;
D.铝的冶炼用电解法,通常采用电解氧化铝制取.
解答 解:A.明矾水溶液中铝离子水解生成具有吸附性氢氧化铝胶体,具有吸附性,能够吸附水中固体杂质颗粒而净水,不具有杀菌消毒作用,家用消毒液含有的次氯酸根离子具有强的氧化性能够杀菌消毒,故A错误;
B.聚乙烯、聚氯乙烯都是高分子化合物,聚氯乙烯受热分解产生有毒物质,不能用于食品包装,故B正确;
C.碳纤维,主要成分为碳单质,属于无机非金属材料,故C错误;
D.一般来说,活泼金属用电解法,铝是活泼金属,所以采用电解法冶炼,故D错误;
故选:B.
点评 本题主要考查运用所学化学知识综合分析和解决实际问题的能力,涉及明矾净水原理、金属的冶炼、材料的分类,明确盐类水解的性质、金属的性质、材料的成分是解题关键,题目难度中等.

练习册系列答案
相关题目
2.将20mL充满NO和NO2的混合气体的试管倒立于盛水的水槽中,充分反应后,剩余气体的体积为10mL,原混合气体中NO体积(气体体积处于同温同压下)( )
| A. | 5 ml | B. | 10 ml | ||
| C. | 15 ml | D. | 条件不足,无法计算 |
3.下列事实一定能证明HNO2是弱电解质的是( )
①常温下NaNO2溶液的pH>7;
②用HNO2溶液做导电实验,灯泡很暗;
③HNO2和NaCl不能发生反应;
④0.1mol/L HNO2溶液的pH=2.1;
⑤NaNO2和H3PO4反应,生成HNO2;
⑥pH=1的 HNO2溶液稀释至100倍,pH约为2.3.
①常温下NaNO2溶液的pH>7;
②用HNO2溶液做导电实验,灯泡很暗;
③HNO2和NaCl不能发生反应;
④0.1mol/L HNO2溶液的pH=2.1;
⑤NaNO2和H3PO4反应,生成HNO2;
⑥pH=1的 HNO2溶液稀释至100倍,pH约为2.3.
| A. | ①④⑥ | B. | ②③④ | C. | 全部 | D. | ①④⑤⑥ |
20.有机化合物A的分子式是C13H20O8(相对分子质量为304),1molA在酸性条件下与4molH2O反应得到4molCH3COOH和1molB.下列说法错误的是( )
| A. | A和B的相对分子质量之差为168 | |
| B. | B一定不能发生加成反应 | |
| C. | 有机物B与CH3CH2OH互为同系物 | |
| D. | 分子式为C5H10O2且与CH3COOH属于同类物质的有机物只有4种 |
7.下列有关实验原理、装置、操作或结论的描述,不正确的是(有关装置的夹持仪器略去未画)( )
| A. | 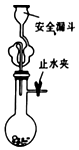 实验室用大理石和盐酸制备二氧化碳 | |
| B. | 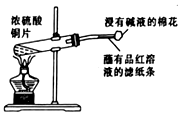 制取SO2、检验SO2的漂白性 | |
| C. | 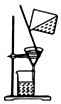 提纯氢氧化铁胶体 | |
| D. | 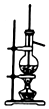 实验室用乙醇和浓硫酸制乙烯 |
2.下列各组离子,能在溶液中大量共存的是( )
| A. | Na+、Mg2+、Cl-、SO42- | B. | Na+、Ca2+、CO32-、NO3- | ||
| C. | Na+、H+、Cl-、CO32- | D. | K+、Al3+、SO42-、OH- |
