题目内容
5.下列关于硫酸性质的描述中,正确的是( )| A. | 浓H2SO4有氧化性,稀H2SO4无氧化性 | |
| B. | 由于浓H2SO4具有脱水性,所以可用做干燥剂 | |
| C. | 稀H2SO4与铜不反应,但浓H2SO4在加热条件下可与铜反应 | |
| D. | 浓硫酸不与铁、铝发生钝化 |
分析 A、稀硫酸中的氢离子具有氧化性;
B、浓硫酸用做干燥剂,是吸水性;
C、浓硫酸具有强氧化性与铜加热的条件下反应;
D、浓硫酸与铁、铝常温下表面形成致密的氧化膜,而发生钝化现象.
解答 解:A、稀硫酸中的氢离子具有氧化性,而不是无氧化性,故A错误;
B、浓硫酸用做干燥剂,是吸水性,而不是脱水性,故B错误;
C、浓硫酸具有强氧化性与铜加热的条件下反应,氢离子是弱氧化剂与铜不反应,故C正确;
D、浓硫酸与铁、铝常温下表面形成致密的氧化膜,而发生钝化现象,故D错误;
故选C.
点评 本题考查浓硫酸的性质,为高考高频考点,侧重于学生的基础知识的综合理解和运用的考查,注意把握浓硫酸的特性以及性质之间的区别,难度不大,注意相关基础的积累.

练习册系列答案
相关题目
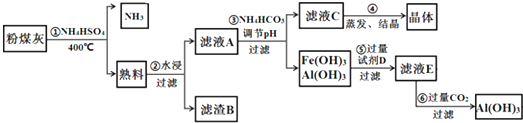
13.辉铜矿石主要含有硫化亚铜(Cu2S)及少量脉石(SiO2).一种以辉铜矿石为原料制备硝酸铜的工艺流程如下:

已知部分阳离子以氢氧化物形式开始沉淀和完全沉淀时溶液的pH如表
(1)写出步骤“还原”中可能发生反应的离子方程式Fe+2Fe3+=3Fe2+、Fe+Cu2+=Cu+Fe2+.
(2)回收S过程中温度控制50℃~60℃之间,不宜过高或过低的原因是温度高苯容易挥发、温度低溶解速率小.
(3)气体NOx与氧气混合后通入水中能生成流程中可循环利用的一种物质,该反应的化学方程式为4NOx+(5-2x)O2+2H2O=4HNO3.
(4)保温除铁过程中加入CuO的目的是调节溶液的pH,使Fe3+完全转化为Fe(OH)3沉淀.
(5)过滤③所得到的滤液,加入硝酸后,经操作X、过滤④得到硝酸铜晶体.硝酸的作用是抑制Cu2+的水解;操作X是蒸发浓缩、冷却结晶(填操作名称).

已知部分阳离子以氢氧化物形式开始沉淀和完全沉淀时溶液的pH如表
| 沉淀物 | Cu(OH)2 | Fe(OH)3 | Fe(OH)2 |
| 开始沉淀pH | 4.7 | 2.7 | 7.6 |
| 完全沉淀pH | 6.7 | 3.7 | 9.6 |
(2)回收S过程中温度控制50℃~60℃之间,不宜过高或过低的原因是温度高苯容易挥发、温度低溶解速率小.
(3)气体NOx与氧气混合后通入水中能生成流程中可循环利用的一种物质,该反应的化学方程式为4NOx+(5-2x)O2+2H2O=4HNO3.
(4)保温除铁过程中加入CuO的目的是调节溶液的pH,使Fe3+完全转化为Fe(OH)3沉淀.
(5)过滤③所得到的滤液,加入硝酸后,经操作X、过滤④得到硝酸铜晶体.硝酸的作用是抑制Cu2+的水解;操作X是蒸发浓缩、冷却结晶(填操作名称).
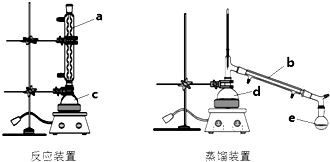
10.某化学兴趣小组利用如图装置进行乙酸乙酯合成和分离的实验探究,请回答以下问题
(1)写出合成乙酸乙酯的化学方程式CH3COOH+CH3CH2OH CH3COOCH2CH3+H2O.
CH3COOCH2CH3+H2O.
(2)仪器b的名称冷凝管,图中起冷凝回流作用的是a(填a、b、c、d、e).
(3)为了提高乙酸乙酯的产率可采取的措施将CH3COOCH2CH3及时蒸馏分离;反应温度不宜过高,减少CH3COOHCH3CH2OH的挥发;反应物控制无水条件,浓硫酸的吸水作用有利于平衡向正反应方向移动,提高产率
(4)经过0.5h加热反应后,将反应装置c中粗产品转移至d中进行蒸馏
根据上表分析,蒸馏后得到的乙酸乙酯中,最有可能含有CH3CH2OH杂质.

(1)写出合成乙酸乙酯的化学方程式CH3COOH+CH3CH2OH
 CH3COOCH2CH3+H2O.
CH3COOCH2CH3+H2O.(2)仪器b的名称冷凝管,图中起冷凝回流作用的是a(填a、b、c、d、e).
(3)为了提高乙酸乙酯的产率可采取的措施将CH3COOCH2CH3及时蒸馏分离;反应温度不宜过高,减少CH3COOHCH3CH2OH的挥发;反应物控制无水条件,浓硫酸的吸水作用有利于平衡向正反应方向移动,提高产率
(4)经过0.5h加热反应后,将反应装置c中粗产品转移至d中进行蒸馏
| 物质 | 98.3%浓硫酸 | 乙酸乙酯 | 乙酸 | 乙醇 | 乙醚 | 水 |
| 沸点 | 338℃, | 77.1℃ | 118℃ | 78.5℃ | 34.6℃ | 100℃ |