题目内容
氢氰酸(HCN)的下列性质中,不能证明它是弱电解质的是( )
| A、1 mol/L氢氰酸溶液的pH约为3 |
| B、常温下,pH=a的HCN稀释100倍后所得溶液pH<(a+2)[(a+2)<7] |
| C、10mL 1mol/L HCN恰好与10mL 1mol/L NaOH溶液完全反应 |
| D、NaCN溶液呈碱性 |
考点:弱电解质在水溶液中的电离平衡
专题:电离平衡与溶液的pH专题
分析:氢氰酸为弱电解质,则利用其电离不完全来分析,一般测定溶液的pH或测定相同条件下与强酸的导电性比较以及对应盐溶液的酸碱性来判断,以此解答该题.
解答:
解:A.氢氰酸为一元酸,0.1mol/L氢氰酸溶液的pH=1时该酸为强酸,但pH约为3,说明电离生成的氢离子约为10-3mol/L<0.1mol/L,电离不完全,故A不选;
B.常温下,pH=a的HCN稀释100倍后所得溶液pH<(a+2),可说明HCN在加水稀释时进一步电离,为弱电解质,故B不选;
C.二者物质的量相等,不能证明酸性的强弱,故C选;
D.NaCN溶液呈碱性,说明为强碱弱酸盐,则HCN为弱酸,故D不选.
故选C.
B.常温下,pH=a的HCN稀释100倍后所得溶液pH<(a+2),可说明HCN在加水稀释时进一步电离,为弱电解质,故B不选;
C.二者物质的量相等,不能证明酸性的强弱,故C选;
D.NaCN溶液呈碱性,说明为强碱弱酸盐,则HCN为弱酸,故D不选.
故选C.
点评:本题考查弱电解质的判断方法,明确弱电解质在水中电离不完全是解答本题的关键,学生应注意在平时的学习中归纳判断弱电解质的方法,难度不大.

练习册系列答案
相关题目
等质量的铜片在酒精灯上热后,分别插入下列液体中,放置片刻后取出,铜片质量不变的是( )
| A、盐酸 | B、乙醇 | C、醋酸 | D、乙醛 |
下列离子方程式中正确的是( )
| A、澄清石灰水与稀盐酸反应Ca(OH)2+2H+═Ca2++2H2O |
| B、氢氧化钡与硫酸反应OH-+H+═H2O |
| C、铜片插入硝酸银溶液中Cu+Ag+═Cu2++Ag |
| D、氯化镁溶液与氢氧化钠溶液反应Mg2++2OH-═Mg(OH)2↓ |
下列叙述不正确的是( )
| A、某溶液中只含Na+、CH3COO-、H+、OH-四种离子,则溶液一定呈现碱性 |
| B、在Na2SO3和NaHSO3混合液中:c(Na+)+c(H+)=c(HSO3-)+c(OH-)+2c(SO32-) |
| C、相同条件下,pH=10的CH3COONa溶液和氨水中,由水电离出的c(OH-)前者大于后者 |
| D、相同物质的量浓度的①CH3COONa溶液②NaNO3溶液③NH4Cl溶液④NaOH溶液,pH的大小顺序是:④>①>②>③ |
下列液体均处于25℃,有关叙述正确的是( )
| A、某物质的溶液pH<7,向该溶液中加入氢氧化钠溶液,Kw增大 |
| B、pH=8的NaOH溶液稀释100倍,其pH=6 |
| C、将1L 0.1mol?L-1的Ba(OH)2溶液稀释为2L,pH=12 |
| D、pH=4.5的番茄汁中c(H+)是pH=6.5的牛奶中c(H+)的100倍 |
下列物质中,肯定是由一种分子构成的物质是( )
| A、糖水 | B、纯净物 | C、混合物 | D、水 |
 对于锌、铜和稀硫酸组成的原电池(如图),下列有关说法正确的是( )
对于锌、铜和稀硫酸组成的原电池(如图),下列有关说法正确的是( )①Zn是负极
②电子由Zn经外电路流向Cu
③Zn-2e-=Zn2+
④溶液中H+向Zn棒迁移.
| A、①② | B、①②③ |
| C、②③④ | D、①②③④ |
下列说法正确的是( )
| A、已知2H2(g)+O2(g)=2H2O(g),△H=-483.6kJ?mol-1,则H2的燃烧热为-241.8kJ?mol-1 | ||||||||||
B、已知:25℃时,
| ||||||||||
C、反应Fe(s)+5CO(g)?Fe(CO)5(g)的平衡常数表达式为K=
| ||||||||||
D、0.1mol?L-1的酒石酸(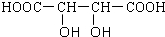 )与0.1mol?L-1的NaOH混合后:c(HC4H4O6-)+2c(C4H4O62-)=c(Na+)+c(H+)-c(OH-) )与0.1mol?L-1的NaOH混合后:c(HC4H4O6-)+2c(C4H4O62-)=c(Na+)+c(H+)-c(OH-) | ||||||||||
在甲、乙两烧杯溶液中,分别含有大量的Cu2+、K+、H+、CO32-、Cl-、OH- 六中离子中的三种,已知乙烧杯中的溶液呈碱性,则甲烧杯中可能含有的离子是( )
| A、Cu2+、H+、Cl- |
| B、CO32-、OH- Cl- |
| C、K+、H+、Cl- |
| D、K+、CO32-、OH- |