题目内容
下列离子方程式中正确的是( )
| A、澄清石灰水与稀盐酸反应Ca(OH)2+2H+═Ca2++2H2O |
| B、氢氧化钡与硫酸反应OH-+H+═H2O |
| C、铜片插入硝酸银溶液中Cu+Ag+═Cu2++Ag |
| D、氯化镁溶液与氢氧化钠溶液反应Mg2++2OH-═Mg(OH)2↓ |
考点:离子方程式的书写
专题:离子反应专题
分析:A.澄清石灰水写离子;
B.二者还反应生成硫酸钡沉淀;
C.电荷不守恒;
D.二者反应生成难溶物氢氧化镁.
B.二者还反应生成硫酸钡沉淀;
C.电荷不守恒;
D.二者反应生成难溶物氢氧化镁.
解答:
解:A.澄清石灰水写离子,离子方程式为OH-+H+═H2O,故A错误;
B.二者还反应生成硫酸钡沉淀,离子方程式为Ba2++SO42-+2OH-+2H+═2H2O+BaSO4↓,故B错误;
C.电荷不守恒,离子方程式为Cu+2Ag+═Cu2++2Ag,故C错误;
D.二者反应生成难溶物氢氧化镁,离子方程式为Mg2++2OH-═Mg(OH)2↓,故D正确;
故选D.
B.二者还反应生成硫酸钡沉淀,离子方程式为Ba2++SO42-+2OH-+2H+═2H2O+BaSO4↓,故B错误;
C.电荷不守恒,离子方程式为Cu+2Ag+═Cu2++2Ag,故C错误;
D.二者反应生成难溶物氢氧化镁,离子方程式为Mg2++2OH-═Mg(OH)2↓,故D正确;
故选D.
点评:本题考查了离子方程式的判断,明确物质间的反应、离子方程式的书写规则即物质的溶解性等知识点即可解答,注意B中易漏掉写水或硫酸钡的离子反应,澄清石灰水写离子、石灰乳写化学式,为易错点.

练习册系列答案
相关题目
体积均为aL的硫酸钾、硫酸锌、硫酸铁溶液,均能和bL1mol/LBaCl2溶液恰好完全反应.则硫酸钾、硫酸锌、硫酸铁的物质的量浓度之比约为( )
| A、3:2:2 |
| B、3:3:1 |
| C、1:3:3 |
| D、1:2:3 |
体积相同、pH值相等的盐酸(甲)和醋酸(乙),分别与锌反应,若最后锌已经全部溶解且放出气体一样多,为此下列说法正确的是( )
| A、反应开始时的速率:甲>乙 |
| B、反应所需时间:甲<乙 |
| C、反应开始时,酸的物质的量浓度:甲>乙 |
| D、反应结束时,pH:甲>乙 |
下列说法中不正确的是( )
| A、Na2O2、HClO、SO2等物质都具有漂白作用 |
| B、液氨、液态氯化氢都是电解质 |
| C、置换反应都是氧化还原反应,复分解反应都是非氧化还原反应 |
| D、明矾能水解生成氢氧化铝胶体,可用作净水剂 |
下列自然、生活中的事例不属于氧化还原反应的是( )
| A、动物呼吸 |
| B、植物光合作用 |
| C、金属生锈 |
| D、石膏点制豆腐 |
氢氰酸(HCN)的下列性质中,不能证明它是弱电解质的是( )
| A、1 mol/L氢氰酸溶液的pH约为3 |
| B、常温下,pH=a的HCN稀释100倍后所得溶液pH<(a+2)[(a+2)<7] |
| C、10mL 1mol/L HCN恰好与10mL 1mol/L NaOH溶液完全反应 |
| D、NaCN溶液呈碱性 |
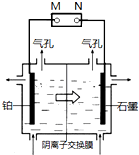 制备单质锰的实验装置如图,阳极以稀硫酸为电解液,阴极以硫酸锰和硫酸混合液为电解液,电解装置中箭头表示溶液中阴离子移动的方向.下列说法不正确的是( )
制备单质锰的实验装置如图,阳极以稀硫酸为电解液,阴极以硫酸锰和硫酸混合液为电解液,电解装置中箭头表示溶液中阴离子移动的方向.下列说法不正确的是( )| A、M是电源的负极 | ||||
| B、左侧气孔逸出的气体可能为副产物H2 | ||||
C、电解槽中发生的总反应为:MnSO4+2H2O
| ||||
| D、若用阳离子交换膜代替阴离子交换膜,阳极可能得到 MnO2 |