题目内容
1.某气态烃的密度是相同状况下氢气密度的28倍.1mol该烃在空气中完全燃烧生成水72g. 求:(1)该烃的相对分子质量.
(2)该烃的分子式.
(3)写出属于烯烃的同分异构体的结构简式.
分析 气态烃的密度是相同状况下氢气密度的28倍,则相对分子质量为56,1mol该烃在空气中完全燃烧生成水72g,可知n(H2O)=$\frac{72g}{18g/mol}$=4mol,则1mol烃含有8molH,结合相对分子质量可确定C原子数,进而确定分子式和结构简式.
解答 解:(1)气态烃的密度是相同状况下氢气密度的28倍,则相对分子质量为28×2=56,
答:该烃的相对分子质量为56;
(2)1mol该烃在空气中完全燃烧生成水72g,可知n(H2O)=$\frac{72g}{18g/mol}$=4mol,则1mol烃含有8molH,则N(C)=$\frac{56-8}{12}$=4,则分子式为C4H8,
答:该烃的分子式为C4H8;
(3)分子式为C4H8,如为烯烃,则对应的结构简式有CH2=CHCH2CH3、CH2=C(CH3)CH3、CH3CH=CHCH3,
答:属于烯烃的同分异构体的结构简式有CH2=CHCH2CH3、CH2=C(CH3)CH3、CH3CH=CHCH3.
点评 本题考查了有机物分子式、结构简式的确定,侧重考查学生的分析能力和计算能力,题目难度中等,注意掌握质量守恒定律在确定有机物分子式中的应用方法,明确同分异构体的概念及书写原则.

练习册系列答案
相关题目
16.某科研小组设计出利用工业废酸(10%H2SO4)来堆浸某废弃的氧化铜锌矿制取活性ZnO的方案,实现废物综合利用,方案如图所示.

已知:298K时各离子开始沉淀及完全沉淀时的pH如表所示.
请回答下列问题:
(1)氧化铜锌矿中含有少量的CuS和ZnS,在H2SO4的作用下ZnS可以溶解而CuS不溶,这是由于相同温度下:Ksp(CuS)<Ksp(ZnS)(选填“>”“<”或“=”).
(2)你认为在除铁过程中选用下列物质中的C(填序号)作为试剂甲是比较合适的.
A.KMnO4 B.HNO3 C.H2O2 D.Cl2
(3)除铁过程中加入氨水的目的是调节溶液的pH,pH应控制在3.2~6.2范围之间.
(4)请写出加甲物质后,加入氨水控制调节溶液的pH下生成Fe(OH)3反应的离子方程式Fe3++3NH3•H2O═Fe﹙OH)3↓+3NH4+.
(5)298K时,残留在乙溶液中的c(Fe3+)在2.7×10-15.6mol/L以下.[Fe(OH)3的Ksp=2.70×10-39].

已知:298K时各离子开始沉淀及完全沉淀时的pH如表所示.
| 离子 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe2+ | 6.34 | 9.7 |
| Fe3+ | 1.48 | 3.2 |
| Zn2+ | 6.2 | 8.0 |
(1)氧化铜锌矿中含有少量的CuS和ZnS,在H2SO4的作用下ZnS可以溶解而CuS不溶,这是由于相同温度下:Ksp(CuS)<Ksp(ZnS)(选填“>”“<”或“=”).
(2)你认为在除铁过程中选用下列物质中的C(填序号)作为试剂甲是比较合适的.
A.KMnO4 B.HNO3 C.H2O2 D.Cl2
(3)除铁过程中加入氨水的目的是调节溶液的pH,pH应控制在3.2~6.2范围之间.
(4)请写出加甲物质后,加入氨水控制调节溶液的pH下生成Fe(OH)3反应的离子方程式Fe3++3NH3•H2O═Fe﹙OH)3↓+3NH4+.
(5)298K时,残留在乙溶液中的c(Fe3+)在2.7×10-15.6mol/L以下.[Fe(OH)3的Ksp=2.70×10-39].
11.能正确表示下列反应的离子方程式是( )
| A. | 向Al2(SO4)3溶液中加入过量的NH3•H2O:Al3++4 NH3•H2O═[Al(OH)4]-+4NH4+ | |
| B. | 用高锰酸钾标准溶液滴定草酸:2MnO4-+16H++5C2O42-═2Mn2++10CO2↑+8H2O | |
| C. | 向CuSO4溶液中加入Na2O2:2Na2O2+2Cu2++2H2O═4Na++2Cu(OH)2↓+O2↑ | |
| D. | 明矾溶液中滴入Ba(OH)2溶液使SO42-恰好完全沉淀:2Ba2++3OH-+Al3++2SO42-═2BaSO4↓+Al(OH)3↓ |
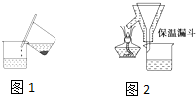


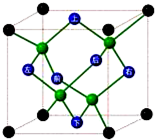 A、B、C、D、E、F六种元素的原子序数依次递增.已知:
A、B、C、D、E、F六种元素的原子序数依次递增.已知: cm,则晶体的密度为$\frac{ρ}{64}$g/cm3.
cm,则晶体的密度为$\frac{ρ}{64}$g/cm3.