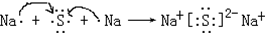题目内容
2.用质量相同的铁单质与下列条件下相同体积的硫酸反应时,生成氢气速率最快的是( )| A. | 20℃铁片 1mol/L硫酸 | B. | 30℃铁粉 1mol/L硫酸 | ||
| C. | 30℃铁粉 2mol/L硫酸 | D. | 30℃铁片 18mol/L硫酸 |
分析 温度越高、浓度越大、接触面积越大,则反应速率越快,以此来解答.
解答 解:由温度可知,A中反应速率最慢,D中为浓硫酸,发生氧化还原反应不生成氢气;
B与C比较,C中氢离子浓度大,反应速率快,
故选C.
点评 本题考查化学反应速率的影响因素,为高频考点,把握温度、浓度对反应速率的影响为解答的关键,侧重分析与应用能力的考查,注意选项D为易错点,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
9.医学上,科学家们设计以Pt和Zn为电极材料的电池,植入人体内作为心脏病患者的心脏起搏器的能源,它依靠人体内体液中存在的一定浓度的溶解的O2、H+、Zn2+进行工作.下列叙述正确的是( )
| A. | Pt为负极,Zn为正极 | |
| B. | Zn为负极,Pt为正极 | |
| C. | 负极反应式为Zn-2e-═Zn2+,正极反应式为2H++2e-═H2↑ | |
| D. | 负极反应式为Zn-2e-═Zn2+,正极反应式为O2+2H2O+4e-═4OH- |
10.用苦卤(含Na+、K+、Mg2+、Cl-、Br-等)可提取溴,其生产流程如下:

则下列说法中,错误的是( )

则下列说法中,错误的是( )
| A. | 反应③的离子方程式为5Br-+BrO3-+6H+═3Br2+3H2O | |
| B. | ②③的目的是富集溴,提高Br2的浓度 | |
| C. | 蒸馏塔温度控制在90℃左右的原因是防止温度过高将水蒸馏出来 | |
| D. | 从海水中提取任何化学物质都需要经过化学变化 |
17.下列有关能量变化的说法正确的是( )
| A. | 2SO2(g)+02(g) $?_{500℃}^{V_{2}O_{5}}$2SO3(g)△H=-196.6 kJ/mol,则2molSO2完全反应放出热量等于196.6kJ | |
| B. | “冰,水为之,而寒于水”说明相同质量的水和冰相比较,冰的能量高 | |
| C. | 已知C(s,石墨)=C(s,金刚石)△H=+1.9 kJ/mol,则金刚石比石墨稳定 | |
| D. | 氢气的燃烧热为285.8 kJ/mol,则氢气燃烧的热化学方程式为:2H2(g)+O2(g)═2H2O(l)△H=-285.8 kJ/mol |
14.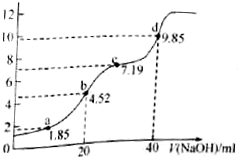 已知:pKa=-LgKa,25℃时,H2SO3的pKa1=1.85,pKa2=7.19.用0.1mol/L NaOH溶液滴定20mL0.1mol/L H2SO3溶液的滴定曲线如图所示(曲线上的数字为pH).下列说法不正确的是( )
已知:pKa=-LgKa,25℃时,H2SO3的pKa1=1.85,pKa2=7.19.用0.1mol/L NaOH溶液滴定20mL0.1mol/L H2SO3溶液的滴定曲线如图所示(曲线上的数字为pH).下列说法不正确的是( )
 已知:pKa=-LgKa,25℃时,H2SO3的pKa1=1.85,pKa2=7.19.用0.1mol/L NaOH溶液滴定20mL0.1mol/L H2SO3溶液的滴定曲线如图所示(曲线上的数字为pH).下列说法不正确的是( )
已知:pKa=-LgKa,25℃时,H2SO3的pKa1=1.85,pKa2=7.19.用0.1mol/L NaOH溶液滴定20mL0.1mol/L H2SO3溶液的滴定曲线如图所示(曲线上的数字为pH).下列说法不正确的是( )| A. | a点所得溶液中:2c(H2SO3)+c(SO32-)<0.1 mol/L | |
| B. | b点所得溶液中:c(H2SO3)+c(H+)=c(SO32-)+c(OH-) | |
| C. | C点所得溶液中:2c(Na+)=3c(HSO3-) | |
| D. | d点所得溶液中:c(Na+)>c(SO32-)>c(HSO3-) |
11.下列反应中属于加成反应的是( )
| A. | 乙烯使溴水褪色 | |
| B. | 将苯滴入溴水中,振荡后水层接近无色 | |
| C. | 乙烯使酸性KMnO4溶液褪色 | |
| D. | 甲烷与氯气混合,黄绿色消失 |
12.用一种试剂鉴别乙醇、苯、1-己烯、苯酚溶液,可选用的试剂是( )
| A. | 溴水 | B. | 氯化铁溶液 | C. | 高锰酸钾溶液 | D. | 四氯化碳 |
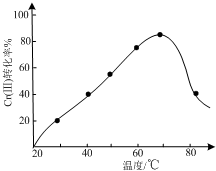 工业含铬废水的处理原理是将Cr2O72-转化为Cr3+,再将Cr3+转化为Cr(OH)3沉淀.利用硫酸工业废气中的SO2处理含铬废水,既充分利用资源、以废治废,还能节约生产成本.
工业含铬废水的处理原理是将Cr2O72-转化为Cr3+,再将Cr3+转化为Cr(OH)3沉淀.利用硫酸工业废气中的SO2处理含铬废水,既充分利用资源、以废治废,还能节约生产成本.