题目内容
有关铜-锌-稀硫酸构成的原电池中的一些说法正确的是( )
| A、锌片为正极,且锌片逐渐溶解 |
| B、铜片为负极,且铜片上有气泡 |
| C、溶液中的H+移向铜极 |
| D、该电池工作的过程中溶液的pH始终不变 |
考点:原电池和电解池的工作原理
专题:
分析:铜-锌-稀硫酸构成的原电池中,锌是负极,负极上锌失电子发生氧化反应,铜为正极,正极上氢离子得电子发生还原反应,电子从负极沿导线流向正极,结合原电池定义分析解答.
解答:
解:锌比铜活泼,形成原电池时,锌为负极,被以后而逐渐溶解,铜为正极,则A、B错误;
原电池工作时,阳离子向正极移动,阴离子向负极移动,正极生产氢气,氢离子浓度逐渐减小,则pH增大,则C正确、D错误.
故选C.
原电池工作时,阳离子向正极移动,阴离子向负极移动,正极生产氢气,氢离子浓度逐渐减小,则pH增大,则C正确、D错误.
故选C.
点评:本题综合考查原电池知识,为高频考点,侧重于学生的分析能力的考查,注意把握原电池组成以及工作原理,难度不大.

练习册系列答案
相关题目
下列对于金属的相关说法正确的是( )
| A、金属都呈银白色,易导电,易导热 |
| B、化合物中金属元素只显正价 |
| C、金属都能与氢氧化钠溶液反应 |
| D、金属都能与盐酸反应 |
下列事实不能用勒沙特列原理解释的是( )
| A、开启啤酒瓶后,瓶中马上泛起大量泡沫 |
| B、由H2、I2(g)、HI(g)气体组成的平衡体系加压后颜色变深 |
| C、实验室常用排饱和食盐水的方法收集氯气 |
| D、工业上生产硫酸的过程中使用过量的空气以提高二氧化硫的利用率 |
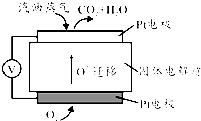
 用气体传感器可以检测汽车尾气中CO的含量.传感器是以燃料电池为工作原理,其装置如图所示,该电池中电解质为氧化钇-氧化钠,其中O2-可以在固体介质NASICON中自由移动.下列说法正确的是( )
用气体传感器可以检测汽车尾气中CO的含量.传感器是以燃料电池为工作原理,其装置如图所示,该电池中电解质为氧化钇-氧化钠,其中O2-可以在固体介质NASICON中自由移动.下列说法正确的是( )| A、燃料电池工作时,电极b作负极 |
| B、工作时,电流由负极通过传感器流向正极 |
| C、b电极的电极反应式为:O2+2H2O+4e-═4OH- |
| D、当消耗11.2L(标准状况下)CO时,理论上传感器中会通过NA个电子 |
设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A、常温常压下,56g乙烯和丙烯的混合气中含有的碳原子数为4NA |
| B、156g Na2O2固体与足量的二氧化碳反应时,转移的电子数为4NA |
| C、将1.06克Na2CO3固体溶于水,溶液中含CO32-数目为0.01NA |
| D、标准状况下,向溶有2.24LSO2的水溶液中,通入3.36LCl2,转移电子数目0.2NA |
同体积、同物质的量浓度的几种可溶性盐的溶液中,一定含有相同的( )
| A、溶质的物质的量 |
| B、溶质的质量 |
| C、酸根离子数 |
| D、金属离子数 |