题目内容
下列对于金属的相关说法正确的是( )
| A、金属都呈银白色,易导电,易导热 |
| B、化合物中金属元素只显正价 |
| C、金属都能与氢氧化钠溶液反应 |
| D、金属都能与盐酸反应 |
考点:常见金属元素的单质及其化合物的综合应用
专题:
分析:金属在化学反应中一般表现为还原性,可失去电子,不同金属的活泼性不同,不一定具有银白色、不一定能与盐酸、氢氧化钠反应,以此解答.
解答:
解:A.金属不一定为银白色,如铜,故A错误;
B.金属在反应中只能失去电子,表现为正价,故B正确;
C.常见能与氢氧化钠溶液反应的金属有铝等,很多金属与氢氧化钠不反应,故C错误;
D.金属活动顺序表中氢以后的金属与盐酸不反应,故D错误.
故选B.
B.金属在反应中只能失去电子,表现为正价,故B正确;
C.常见能与氢氧化钠溶液反应的金属有铝等,很多金属与氢氧化钠不反应,故C错误;
D.金属活动顺序表中氢以后的金属与盐酸不反应,故D错误.
故选B.
点评:本题考查金属的性质,为高频考点,侧重双基的考查,注意相关基础知识的积累,难度不大.

练习册系列答案
相关题目
已知热化学方程式:SO2(g)+
O2(g)?SO3(g)△H=-98.3kJ?mol-1,现有4molSO2参加反应,当放出314.3kJ热量时,约剩余SO2的物质的量为( )
| 1 |
| 2 |
| A、1.4mol |
| B、2.6mol |
| C、0.8mol |
| D、1mol |
要除去Fe2O3中混有的Al2O3,最好的方法是( )
| A、用NaOH洗涤、过滤 |
| B、用H2加热还原 |
| C、用CO加热还原 |
| D、用盐酸洗涤过滤 |
下列各组离子在所给条件下能够大量共存的是( )
| A、pH=0的溶液中,Fe3+、Mg2+、Cl-、SO42- |
| B、水电离出的c(H+)=1×10-13mol?L-1的溶液中,K+、HCO3-、Cl-、S2- |
| C、使pH试纸显深蓝色的溶液中,Cu2+、NO3-、Fe3+、SO42- |
| D、在AlCl3溶液中,Na+、AlO2-、NO3-、SO42- |
下列排列顺序正确的是( )
| A、常温下将0.1 mol?L-1 CH3COONa溶液与0.05 mol?L-1 HCl溶液等体积混合,c (Na+)>c (Cl-)>c(CH3COO-)>c (OH-)>c (H+) |
| B、常温下物质的量浓度相等的①NH4HSO4;②(NH4 )2CO3;③NH4Cl三种溶液中c(NH4+):①>③>② |
| C、常温下0.1mol?L-1的NaHA溶液,其pH=11,则溶液中:c(HA-)>c(OH-)>c(A2-)>c(H2A) |
D、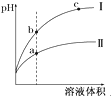 某温度下,相同pH的酸Ⅰ和酸Ⅱ溶液分别加水稀释,pH随溶液体积变化的曲线如图所示.据图判断相同条件下酸性:Ⅰ>Ⅱ 某温度下,相同pH的酸Ⅰ和酸Ⅱ溶液分别加水稀释,pH随溶液体积变化的曲线如图所示.据图判断相同条件下酸性:Ⅰ>Ⅱ |
要验证Mg、Fe、Cu三种金属的活动性顺序,可选用下列哪组物质进行实验( )
| A、Cu、FeCl2溶液、MgCl2溶液 |
| B、Fe、Cu、MgCl2溶液 |
| C、Mg、CuO、FeSO4溶液 |
| D、Fe、CuSO4溶液、MgCl2溶液 |
有关铜-锌-稀硫酸构成的原电池中的一些说法正确的是( )
| A、锌片为正极,且锌片逐渐溶解 |
| B、铜片为负极,且铜片上有气泡 |
| C、溶液中的H+移向铜极 |
| D、该电池工作的过程中溶液的pH始终不变 |