题目内容
7.下列反应中,需要加入氧化剂才能发生的是( )| A. | HNO3→NO | B. | H2SO4 (浓)→SO2 | C. | I-→I2 | D. | Br2→Br- |
分析 需要加入氧化剂才能实现,则选项中为还原剂的反应,还原剂中某元素的化合价升高被氧化,以此来解答.
解答 解:A.HNO3→NO中N元素的化合价降低,则需要加还原剂才能实现,故A不选;
B.H2SO4 (浓)→SO2中S元素的化合价降低,则需要加还原剂才能实现,故B不选;
C.I-→I2中I元素的化合价升高,则需要加氧化剂才能实现,故C选;
D.Br2→Br-中Br元素的化合价降低,则需要加还原剂才能实现,故D不选;
故选C.
点评 本题考查氧化还原反应,题目难度不大,明确元素的化合价及反应中化合价的变化是解答本题的关键,注意掌握氧化剂、还原剂的概念及判断方法.

练习册系列答案
相关题目
10.下列各组中,在一定条件下前面的元素可以把后面的元素从其化合物的溶液中置换出来的是( )
| A. | Cu、Fe、Ag | B. | Cl、Br、I | C. | Na、Cu、Hg | D. | F、Br、I |
18. 下列气体中,在实验室能用如图所示的装置制取并收集的是( )
下列气体中,在实验室能用如图所示的装置制取并收集的是( )
 下列气体中,在实验室能用如图所示的装置制取并收集的是( )
下列气体中,在实验室能用如图所示的装置制取并收集的是( )| A. | H2 | B. | NH3 | C. | O2 | D. | CO2 |
15.如图是一些常见有机物的转化关系,关于反应①~⑦的说法不正确的是( )
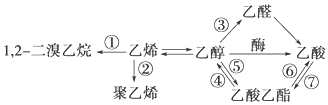

| A. | 反应①是加成反应 | B. | 只有反应②是加聚反应 | ||
| C. | 只有反应⑦是取代反应 | D. | 反应③是氧化反应 |
2.下列事实与胶体性质无关的是( )
| A. | 豆浆加入盐卤做豆腐 | B. | 工厂采用静电除尘 | ||
| C. | CuSO4与NaOH溶液混合产生沉淀 | D. | 血液透析 |
12.下列有关金属钠及其化合物的说法中,错误的是( )
| A. | Na2O是淡黄色固体,和水反应生成NaOH,是碱性氧化物 | |
| B. | 钠应保存于煤油中 | |
| C. | 钠投入滴有紫色石蕊试液的水中,溶液呈现红色 | |
| D. | 钠的焰色为黄色 |
19.下列说法正确的是( )
| A. | 根据能量守恒定律,反应物的总能量一定等于生成物的总能量 | |
| B. | 强、弱电解质的本质区别是溶解度的大小不同 | |
| C. | 在海轮外壳连接锌块保护外壳不受腐蚀 | |
| D. | 室温下,在蒸馏水中滴入少量盐酸后,溶液的PH增大 |
16.已知:2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l);△H=-1451.6kJ•mol-1.下列叙述正确的是( )
| A. | 该反应是吸热反应 | |
| B. | 2mol甲醇所具有的能量是1451.6 kJ | |
| C. | 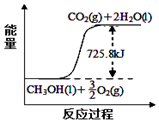 如图是CH3OH(l)燃烧反应过程的能量变化示意图 | |
| D. | 25℃、101kPa时,1 mol甲醇完全燃烧生成CO2和液态水,同时放出725.8 kJ热量 |
17.NA为表阿伏加德罗常数的值,下列说法不正确的是( )
| A. | 9 g38903Sr2+中含有的电子数为3.6 NA | |
| B. | 某温度下纯水的pH=6,该温度下1L pH=11的NaOH溶液中含OH-的数目为0.1NA | |
| C. | 一定温度下,1 L 0.5 mol•L-1 NH4Cl溶液与2 L 0.25 mol•L-1NH4Cl溶液含NH4+均为0.5NA | |
| D. | 丙烯和环丙烷组成的42 g混合气体中氢原子的个数为6NA |